题目内容
同温同压下,A容器中H2和B容器中NH3所含原子总数相等(两个容器中均只有一种气体),则A、B两容器的容积之比为( )
| A、1:2 | B、2:1 |
| C、2:3 | D、1:1 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:同温同压下,气体摩尔体积相等,A容器中H2和B容器中NH3所含原子总数相等,根据分子构成知,氢气和氨气的分子个数之比=2:1,根据V=nVm=
Vm确定二者体积之比.
| N |
| NA |
解答:
解:同温同压下,气体摩尔体积相等,A容器中H2和B容器中NH3所含原子总数相等,根据分子构成知,氢气和氨气的分子个数之比=2:1,根据V=nVm=
Vm知二者体积之比等于其分子个数之比,为2:1,
故选B.
| N |
| NA |
故选B.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,会根据原子个数之比计算分子个数之比,为易错点.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
日本福岛核电站发生核泄漏,对周围土地、海域产生影响.我国东部沿海地区先后检测出放射性物质
I,含量较低,对人们的生活、健康没有造成影响.下列对
I的叙述错误的是( )
131 53 |
131 53 |
A、
| ||||
| B、I元素的相对原子质量为131 | ||||
C、
| ||||
D、
|
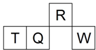 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与主族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与主族序数相等.下列判断不正确的是( )| A、R元素的最简单气态氢化物极易溶于水 |
| B、最高价氧化物对应水化物的酸性:W>Q |
| C、原子半径:T>R |
| D、含T元素的盐溶液一定显碱性 |
H2A是二元弱酸,KHA溶液呈酸性.在0.1mol?L-1KHA溶液中,下列关系正确的是( )
| A、c(K+)+c(H+)═c(HA-)+c(OH-)+c(A2-) |
| B、c(HA-)+c(A2-)=0.1 mol?L-1 |
| C、c(A2-)>c(H2A) |
| D、c(K+)═c(H2A)+c(HA-)+c(A2-) |
在48g碳不完全燃烧所得气体中,CO、CO2均占
体积,且C(s)+
O2(g)═CO(g)△H=-110.5kJ?mol-1;CO(g)+
O2(g)═CO2(g)△H=-283kJ?mol-1.与这些碳完全燃烧相比,损失的热量是( )
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、172.5 kJ |
| B、1 149 kJ |
| C、283 kJ |
| D、566 kJ |
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式不正确的是( )
A、CH3OH(l)+
| ||
| B、2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-1452KJ?mol-1 | ||
| C、2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=+725.8KJ?mol-1 | ||
| D、2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=+1452KJ?mol-1 |
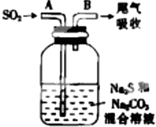 硫、氯及其化合物由广泛的用途.
硫、氯及其化合物由广泛的用途.