题目内容
13.下列与有机物的结构、性质有关的叙述中正确的是( )| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 乙酸与乙醇可发生酯化反应,均可与金属钠发生置换反应 | |
| C. | 分馏、干馏都是物理变化,裂化、裂解都是化学变化 | |
| D. | 石油经过分馏得到多种烃,煤经过分馏可制焦炭、煤焦油等 |
分析 A.乙烯、氯乙烯均含碳碳双键,而聚乙烯不含双键;
B.乙醇含-OH,乙酸含-COOH,均与Na反应生成氢气,二者可发生酯化反应;
C.干馏生成煤焦油等,裂解、裂化均为大分子转化为小分子的反应;
D.煤经过干馏可制焦炭、煤焦油等.
解答 解:A.乙烯、氯乙烯均含碳碳双键,而聚乙烯不含双键,则只有乙烯、氯乙烯可使酸性高锰酸钾溶液褪色,故A错误;
B.乙醇含-OH,乙酸含-COOH,均与Na反应生成氢气,均为置换反应,且二者可发生酯化反应生成乙酸乙酯,故B正确;
C.干馏生成煤焦油等,裂解、裂化均为大分子转化为小分子的反应,均为化学变化,而分馏为物理变化,故C错误;
D.煤经过干馏可制焦炭、煤焦油等,分馏与混合物的沸点有关,为物理变化,则石油经过分馏得到多种烃,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意煤和石油的综合应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列各项化学用语中表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | CH4分子的比例模型 | ||
| C. | 硫离子的结构示意图: | D. | 氮气的电子式 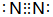 |
4.氰气[(CN)2]和氰化物都是剧毒性物质,氰分子的结构式为N≡C-C≡N,性质与卤素相似,下列叙述错误的是( )
| A. | 氰分子中四原子共直线,是非极性分子 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
8. 脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
 脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )| A. | 脱落酸在一定条件下能和乙酸发生酯化反应 | |
| B. | 脱落酸分子中含有4个甲基 | |
| C. | 等量脱落酸与足量的NaHCO3、Na反应,放出CO2与H2的物质的量之比为n(CO2):n(H2)=2:1 | |
| D. | 脱落酸能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色 |
18.化学与生产、生活、社会可持续发展密切相关.下列说法正确的是( )
| A. | 推广使用一次性木筷,减少疾病传染 | |
| B. | 将地沟油回收重新加工为食用油,提高资源的利用率 | |
| C. | 推广使用电动汽车、天然气汽车等公共交通工具,保护环境 | |
| D. | 推广使用煤的气化、液化技术可减少二氧化碳等温室气体的排放 |
5.Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见无机化合物.下列说法不正确的是( )
| A. | 简单离子半径:Z>W>X>Y | |
| B. | W、X形成的化合物中一定含有离子键 | |
| C. | 最简单氢化物的还原性:Z>W | |
| D. | 工业上常用电解熔融氯化物的方法制备X、Y的单质 |
17.中学化学常见物质A、B、C、D、X、Y,存在如图转化关系(部分物质和条件略去)请根据要求回答下列问题:

(1)若A为NaOH溶液,X为CO2,D是沉淀,①则Y可为BD(填序号).
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
②A可与C反应生成B的离子方程式为HCO3-+OH-=CO32-+H2O.
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,A与D反应生成一种化肥,
①实验室制备气体A的反应、收集和尾气处理装置如图依次为ACG.用此装置制备A的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.

②写出木炭与D的浓溶液在加热的条件下发生反应的化学方程式4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+4NO2↑.
(3)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,
①检验B溶液中是否存在C的试剂可选用C(填序号).
A.Cl2 B.NaOH溶液 C.酸性KMnO4 D.KSCN溶液
②C溶液在贮存时应加入少量X,其理由是(用离子方程式说明)2Fe3++Fe=3Fe2+.
(4)若A金属,D为强碱,则:
①写出A与水反应生成D的离子方程式2Na+2H2O=2Na++2OH-+2H2↑.
②反应Ⅲ中,还原剂是Na2O2.
(5)若A为淡黄色固体单质,D是强酸,
①把一定量的锌与100mL 18.5mol•L-1的D充分反应后,锌完全溶解,同时生成气体M 33.6L(标准状况).将反应后的溶液稀释到1L后溶液的c(H+)=0.1mol•L-1,则下列叙述不正确的是B.
②为了分离气体M,并分别得到干燥的气体,某学生设计了如图实验装置,a、b为活塞,且每个装置中的溶液均过量.甲容器中盛C;乙容器中盛A(填字母).
A.浓硫酸 B.稀硫酸 C.氢氧化钠溶液 D.氯化钡溶液

气体M实验时,关闭b,打开a,此时分离出的气体是H2;当分离完一种气体后,关闭a,打开b,此时得到的气体是SO2.

(1)若A为NaOH溶液,X为CO2,D是沉淀,①则Y可为BD(填序号).
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
②A可与C反应生成B的离子方程式为HCO3-+OH-=CO32-+H2O.
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,A与D反应生成一种化肥,
①实验室制备气体A的反应、收集和尾气处理装置如图依次为ACG.用此装置制备A的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.

②写出木炭与D的浓溶液在加热的条件下发生反应的化学方程式4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+4NO2↑.
(3)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,
①检验B溶液中是否存在C的试剂可选用C(填序号).
A.Cl2 B.NaOH溶液 C.酸性KMnO4 D.KSCN溶液
②C溶液在贮存时应加入少量X,其理由是(用离子方程式说明)2Fe3++Fe=3Fe2+.
(4)若A金属,D为强碱,则:
①写出A与水反应生成D的离子方程式2Na+2H2O=2Na++2OH-+2H2↑.
②反应Ⅲ中,还原剂是Na2O2.
(5)若A为淡黄色固体单质,D是强酸,
①把一定量的锌与100mL 18.5mol•L-1的D充分反应后,锌完全溶解,同时生成气体M 33.6L(标准状况).将反应后的溶液稀释到1L后溶液的c(H+)=0.1mol•L-1,则下列叙述不正确的是B.
| A.气体M是SO2和H2的混合物 | B.气体M是SO2和H2的体积比为4:1 |
| C.反应中共消耗锌97.5g | D.反应中共转移电子3mol |
A.浓硫酸 B.稀硫酸 C.氢氧化钠溶液 D.氯化钡溶液

气体M实验时,关闭b,打开a,此时分离出的气体是H2;当分离完一种气体后,关闭a,打开b,此时得到的气体是SO2.

 为该转化过程的催化剂
为该转化过程的催化剂