题目内容
氢氧燃料电池已用于航天飞机.以30% KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:
2H2+4OH--4e-=4H2O;O2+2H2O+4e-=4OH- 下列说法错误的是( )
2H2+4OH--4e-=4H2O;O2+2H2O+4e-=4OH- 下列说法错误的是( )
| A、氧气通入正极发生氧化反应 |
| B、燃料电池的能量转化率不能达到100% |
| C、供电时的总反应为:2H2+O2=2H2O |
| D、产物为无污染的水,属于环境友好电池 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据电极反应式知,氢氧燃料碱性电池中,通入氢气的电极是负极,氢气被氧化生成水,通入氧气的电极是正极,发生还原反应,电池反应式为2H2+O2=2H2O,以此解答该题.
解答:
解:A.氧气被还原,应为原电池的正极反应,故A错误;
B.氢氧燃料电池是将化学能转变为电能的装置,还会伴有热能等能量的释放,能量转化率不会达100%,故B正确;
C.电池总反应与氢气在氧气中燃烧的化学方程式一致,供电时的总反应为2H2+O2═2H2O,故C正确;
D.氢氧燃料电池产物是水,对环境无污染,且能量转化率高,故D正确.
故选A.
B.氢氧燃料电池是将化学能转变为电能的装置,还会伴有热能等能量的释放,能量转化率不会达100%,故B正确;
C.电池总反应与氢气在氧气中燃烧的化学方程式一致,供电时的总反应为2H2+O2═2H2O,故C正确;
D.氢氧燃料电池产物是水,对环境无污染,且能量转化率高,故D正确.
故选A.
点评:本题考查原电池的组成以及工作原理,题目难度不大,注意电极反应式以及能量的转换形式,注意燃料电池的能量转化率不能达到100%,为易错点.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
一氟一氯丙烷是对臭氧层有严重破坏的一类氟氯代烃,其分子式为C3H6FCl,该物质的同分异构体有(不考虑立体异构)( )
| A、3种 | B、4种 | C、5种 | D、6种 |
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示.下列说法错误的是( )


| A、当左槽溶液逐渐由黄变蓝,其电极反应式为:VO2++2H++e-=VO2++H2O |
| B、充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
| C、放电过程中氢离子通过交换膜定向移入左槽 |
| D、充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为1 mol |
下列化学用语或模型正确的是( )
| A、CO2的结构式:O-C-0 |
B、氟化钠的电子式: |
C、CCl4分子的比例模型: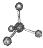 |
D、金刚石的结构模型: |
下列有关说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、0.1NA氮分子所占的体积为2.24L |
| B、标准状况下,2.24L氧气所含分子数为0.1NA |
| C、2.4g镁作还原剂时,失去的电子数为0.2NA |
| D、2mol/L盐酸中,含HCl分子数为0.2NA |
在下列溶液中能大量共存的离子组是( )
| A、Fe3+、Na+、Cl-、SCN- | ||
B、HCO3-、Ca2+、C
| ||
| C、Na+、AlO2-、NO3-、H+ | ||
| D、K+、Na+、Cl-、SO42- |
以石墨做电极,电解1mol/L下列物质的水溶液,下列表述正确的是( )
| A、若为盐酸溶液,pH减小 |
| B、若为氢氧化钠溶液,pH减小 |
| C、若为硫酸钠溶液,pH不变 |
| D、若为氯化钠溶液,pH不变 |