题目内容
某无色溶液中加入过量盐酸有沉淀产生,过滤后向滤液中加入过量氨水又有沉淀产生,下列溶液中符合此条件的是( )
| A、Ag+、Al3+、K+ |
| B、SiO32-、AlO2-、K+ |
| C、Ag+、Cu2+、Na+ |
| D、Ag+、Ba2+、Na+ |
考点:离子共存问题
专题:离子反应专题
分析:溶液无色,则有颜色的离子不能大量共存,加入过量盐酸有沉淀产生,则溶液中可能存在SiO32-或Ag+,加入过量氨水又有沉淀产生,则溶液中可能存在AlO2-或Al3+.
解答:
解:A.加入盐酸可生成AgCl沉淀,过滤后向滤液中加入过量氨水,可生成氢氧化铝沉淀,故A正确;
B.溶液无色,加入盐酸可生成硅酸沉淀,同时生成铝离子,加入过量氨水可生成氢氧化铝沉淀,故B正确;
C.Cu2+有颜色,不符合题目无色要求,故C错误;
D.加入盐酸可生成ACl沉淀,过滤后向滤液中加入过量氨水,没有沉淀生成,故D错误.
故选AB.
B.溶液无色,加入盐酸可生成硅酸沉淀,同时生成铝离子,加入过量氨水可生成氢氧化铝沉淀,故B正确;
C.Cu2+有颜色,不符合题目无色要求,故C错误;
D.加入盐酸可生成ACl沉淀,过滤后向滤液中加入过量氨水,没有沉淀生成,故D错误.
故选AB.
点评:本题考查离子共存问题,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合考查,注意把握题给信息,答题时要注意审题,明确常见离子的性质以及反应类型为解答该类题目的关键,难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列四种化合物:①碳酸氢镁 ②氢氧化铝 ③偏铝酸钠 ④硫化铵,既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A、① | B、②③ | C、②③④ | D、①②④ |
互为同系物的有机物,一定具有( )
| A、相同的分子式 |
| B、相同的相对分子质量 |
| C、相似的结构 |
| D、相同的性质 |
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2;
②向NaAlO2溶液中逐滴加入过量的稀盐酸;
③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硅酸钠溶液中逐滴加入过量的盐酸.
①向饱和碳酸钠溶液中通入过量的CO2;
②向NaAlO2溶液中逐滴加入过量的稀盐酸;
③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硅酸钠溶液中逐滴加入过量的盐酸.
| A、①② | B、①③ | C、①④ | D、②③ |
下列关于胶体的叙述,不正确的是( )
| A、有色玻璃是固溶胶 |
| B、用滤纸能把胶体中的分散质与分散剂分离 |
| C、雾、云、烟都是气溶胶 |
| D、胶体粒子直径大小在1nm~100nm 之间 |
下列关于液氯和氯水的叙述中正确的是( )
| A、液氯是纯净物,而氯水是混合物 |
| B、液氯无酸性,氯水有酸性 |
| C、液氯和氯水都有漂白性 |
| D、液氯无色,氯水呈黄绿色 |
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示)下列有关说法不正确的是( )
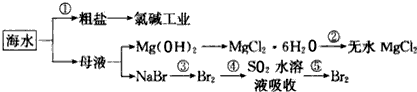
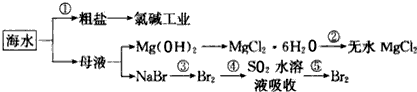
| A、从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程 |
| B、过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| C、过程②中结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| D、在过程③⑤中溴元素均被氧化 |
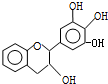 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A、分子中不可能所有的原子共面 |
| B、1mol EGC与4mol NaOH恰好完全反应 |
| C、能发生氧化反应、取代反应和加成反应 |
| D、遇FeCl3溶液不发生显色反应 |