题目内容
11.有碳原子数相同的烯烃、炔烃混合气xL,完全燃烧后生成yLCO2和zL水蒸气(温度、压强和原混合气相同),若x:y:z=3:6:4,则下列叙述正确的是( )| A. | 原混合气为体积比为1:2的乙烯和乙炔 | |
| B. | 原混合气为体积比为1:1的丙烯和丙炔 | |
| C. | 原混合气为任意体积比的乙烯和乙炔 | |
| D. | 原混合气为体积比为1:2的乙烯和丙炔 |
分析 碳原子数相同的烯烃、炔烃混合气xL,完全燃烧后生成yL CO2和zL水蒸气(温度、压强与原混合气相同),若x:y:z=3:6:4,根据原子守恒可知,平均分子式为C2H$\frac{8}{3}$,故根据C原子数目可知,该组成为乙烯与乙炔,再根据平均H原子数目计算二者体积之比.
解答 解:碳原子数相同的烯烃、炔烃混合气xL,完全燃烧后生成yL CO2和zL水蒸气(温度、压强与原混合气相同),若x:y:z=3:6:4,根据原子守恒可知,平均分子式为C2H$\frac{8}{3}$,
根据C原子数目相同可知,该组成为乙烯与乙炔,设乙烯与乙炔的物质的量分别为amol、bmol,则:$\frac{4a+2b}{a+b}$=$\frac{8}{3}$,整理得a:b=1:2,
物质的量之比等于体积之比,所以原混合气体为体积比为1:2的乙烯和乙炔,
故选A.
点评 本题考查混合物的有关计算,题目难度中等,确定平均分子式是解题的关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
1.下列固体物质属于晶体的是( )
| A. | 橡胶 | B. | 食盐 | C. | 石蜡 | D. | 玻璃 |
2.${\;}_{92}^{235}$U是制造原子弹和核发电的重要工业原料,关于铀元素的下列说法正确的是( )
| A. | ${\;}_{\;}^{235}$U的原子核外有143个电子 | B. | ${\;}_{\;}^{235}$U、${\;}_{\;}^{238}$U是同一种核素 | ||
| C. | ${\;}_{\;}^{235}$U一个原子中有92个中子 | D. | ${\;}_{\;}^{235}$U和${\;}_{\;}^{238}$U互为同位素 |
19.有机物种类繁多,有下列8种有机物,有关说法不正确的是( )
①C5H12 ②C3H6 ③CH2=CH-CH=CH2④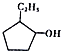 ⑤
⑤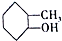 ⑥
⑥ ⑦
⑦ ⑧
⑧
①C5H12 ②C3H6 ③CH2=CH-CH=CH2④
 ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
| A. | ①和⑧是同系物 | B. | ②和③不是同系物 | ||
| C. | ④和⑤是同分异构体 | D. | ⑥和⑦是同分异构体 |
6.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.2mol丙烯酸中含有双键的数目为0.2NA | |
| B. | 丙烯和1-丁烯组成的21g混合气体中氢原子的个数为3NA | |
| C. | 标准状况下,11.2L苯中含有分子的数目为0.5NA | |
| D. | 1mol羟基与1mol氢氧根离子所含电子数均为9NA |
16.草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4的工艺流程如下:
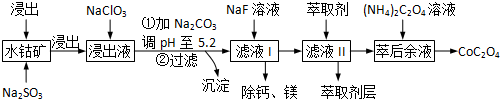
己知:,①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+还原.
(2)NaClO3可将Fe2+氧化为Fe3+离子.可用氯气通入到热的浓氢氧化钠溶液来制取NaClO3.实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为6.72L(标准状况下).
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示.使用萃取剂最适宜的pH是B(填选项序号).
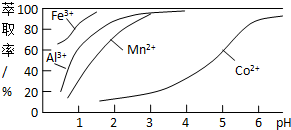
A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知某温度下,Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.
(5)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用c mol/L高锰酸钾溶液去滴定,当溶液由无色变为浅紫色(或紫红色),且半分钟内不变色时(填颜色变化),共用去高锰酸钾溶液VmL,计算草酸钴样品的纯度为36.75cv/m%.

己知:,①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3可将Fe2+氧化为Fe3+离子.可用氯气通入到热的浓氢氧化钠溶液来制取NaClO3.实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为6.72L(标准状况下).
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示.使用萃取剂最适宜的pH是B(填选项序号).

A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知某温度下,Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.
(5)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用c mol/L高锰酸钾溶液去滴定,当溶液由无色变为浅紫色(或紫红色),且半分钟内不变色时(填颜色变化),共用去高锰酸钾溶液VmL,计算草酸钴样品的纯度为36.75cv/m%.
20.某化学科研小组对周围大气进行监测,发现该地区首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx灯进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样品配成待测试样,若测得该试样所含水溶性无机离子的化学组分及平均浓度如下表:
根据表中数据计算该试样的pH=4.
(2))①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a.氨水 b.Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L(NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0.汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,试判断该设想能否实现并简述理由否,因△H>0且△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样品配成待测试样,若测得该试样所含水溶性无机离子的化学组分及平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2))①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a.氨水 b.Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L(NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0.汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,试判断该设想能否实现并简述理由否,因△H>0且△S<0,则在任何温度下△G>0,不可能自发进行.
1.下列说法正确的是( )
| A. | 分子式为C3H6的有机物只有两种同分异构体 | |
| B. | 标准状况下,22.4 L CCl4的质量为154 g | |
| C. | 选用适当的催化剂,既可以改变化学反应速率,也可以改变反应物的平衡转化率 | |
| D. | 2 g H2(g)在O2(g)中完全燃烧生成H2O(l)放出热量为285.8 kJ,则该反应的热化学方程式可表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
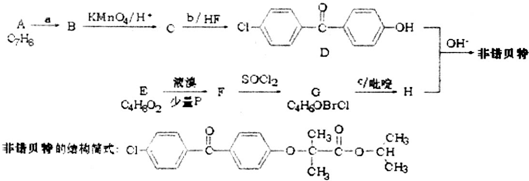
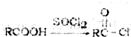
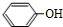 ,F
,F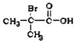 .
. .
. .
. .
.