题目内容
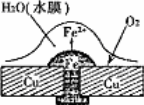
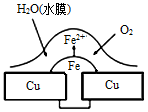
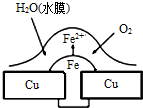
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法中正确的是( )

| A、此过程中铜被腐蚀 | B、此过程中电子从Cu移向Fe | C、正极电极反应式为O2+2H2O+4e-═4OH- | D、铁钉表面发生的反应为Fe-3e-═Fe3+ |
分析:铜、铁和溶有氧气的水构成原电池,铁易失电子作负极,铜作正极,负极上铁发生氧化反应,正极上氧气得电子发生还原反应,电子从负极流向正极.
解答:解:A.该装置构成原电池,铁易失电子作负极,铜作正极,所以铜被保护,故A错误;
B.电子从负极铁流向正极铜,故B错误;
C.正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,故C正确;
D.负极铁失电子生成亚铁离子,电极反应式为Fe-2e-═Fe2+,故D错误;
故选C.
B.电子从负极铁流向正极铜,故B错误;
C.正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,故C正确;
D.负极铁失电子生成亚铁离子,电极反应式为Fe-2e-═Fe2+,故D错误;
故选C.
点评:本题考查了原电池原理,根据金属的活动性判断正负极,再结合电极反应来分析解答即可,易错选项是D,注意铁失电子生成亚铁离子而不是铁离子,为易错点.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
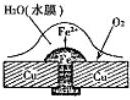 铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法错误的是( )
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法错误的是( )| A、正极电极反应式为:2H++2e-=H2↑ | B、此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 | C、此过程中铁先被腐蚀 | D、此过程中电子由铜板向铁 |