题目内容
11.我国科学家研制出一种催化剂能在室温下高效催化氧化空气中的甲醛,其反应如下:HCHO+O2 $\frac{\underline{\;催化剂\;}}{\;}$CO2+H2O.下列有关说法正确的是( )| A. | 反应中甲醛体现氧化性 | B. | CO2分子中的化学键为非极性键 | ||
| C. | 每生成1.8gH2O消耗2.24L O2 | D. | HCHO分子中α键和π键的比例为3:1 |
分析 A.得氧的反应为氧化反应;
B.不同非金属元素间形成非极性键,同种非金属元素间形成极性键;
C.气体的体积与温度、压强有关;
D.一个单键就是一个α键,一个双键就是一个α键,一个π键.
解答 解:A.得氧的反应为氧化反应,该反应为氧化反应,甲醛被氧化,体现了还原性,故A错误;
B.不同非金属元素间形成非极性键,同种非金属元素间形成极性键,CO2中只存在C=O极性键,故B错误;
C.不能标准状况,无法计算氧气的体积,故C错误;
D.甲醛中,含有碳氧双键以及两个碳氢单键,故其中3个α键,1个π键,即分子中α键和π键的比例为3:1,故D正确.
故选D.
点评 本题以除甲醛气体为新的知识情境,考查了化学反应基本理论和基本概念,涉及氧化还原反应,分子结构、化学键以及气体的体积等相关知识,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
2.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3 NA | |
| B. | 1 L 1 mol•L-1氨水中,NH4+和OH-总数为2NA | |
| C. | 常温常压下,6 0g 二氧化硅含有的氧原子数目为2NA | |
| D. | 22.4LCl2与足量的FeCl2溶液充分反应转移的电子数为2NA |
19.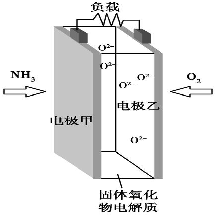 科技工作者研究出以NH3为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )
科技工作者研究出以NH3为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )
 科技工作者研究出以NH3为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )
科技工作者研究出以NH3为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )| A. | 电极甲为电池正极 | |
| B. | 电池总反应为4NH3+5O2═4NO+6H2O | |
| C. | 电池正极反应式为O2+2H2O+4e-═4OH- | |
| D. | 图示中的O2-由电极乙移向电极甲 |
6.能区分胶体和溶液的方法是( )
| A. | 静置,有沉淀现象的是胶体 | B. | 能透过滤纸的是溶液 | ||
| C. | 用肉眼观察,均匀透明的是溶液 | D. | 有丁达尔现象的是胶体 |
16.下列分离混合物的操作中,必须加热的是( )
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
1.下列说法中正确的是( )
| A. | 摩尔既是物质的数量单位又是物质的质量单位 | |
| B. | 物质的量是国际单位制中七个基本单位之一 | |
| C. | 阿伏加德罗常数是0.012kg 12C中含有的碳原子数目 | |
| D. | 标准状况下,1molH2O所占的体积为22.4L |