题目内容
下列有关氧化还原反应的说法正确的是
A.2Na2O2+2H2O=4NaOH+O2? 反应中,Na2O2是氧化剂,H2O是还原剂
B.KClO3+6HCl=KCl+3Cl2?+3H2O 反应中,被氧化的氯元素与被还原的氯元素质量比为6:1
C.KClO3+6HCl=KCl+3Cl2?+3H2O 反应中,转移的电子数为6e-
D.CaH2+2H2O=Ca(OH)2+2H2? 反应中,Ca(OH)2既不是氧化产物也不是还原产物
D
【解析】
试题分析:A、反应中,Na2O2即是氧化剂,又是还原剂,错误;B、反应中,被氧化的氯元素与被还原的氯元素质量比为5:1 ,错误;C、反应中,转移的电子数为5e- ,错误;D、反应中,Ca(OH)2中各元素化合价没有变化,既不是氧化产物也不是还原产物,正确。答案选D。
考点:化还原反应

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案(12分)在100 ℃时,将0.100 mol N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(1)该反应的平衡常数表达式为________;从表中分析:
c1________c2,c3________c4(填“>”、“<”或“=”)。
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为________mol·L-1·s-1。
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是________(填字母序号)。
A.扩大容器的容积
B.再充入一定量的N2O4
C.分离出一定量的NO2
D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080 mol NO2气体,则达到平衡时NO2气体的转化率为________。
 Cu(OH)2?+Na2CO3
Cu(OH)2?+Na2CO3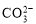 =CaCO3? , Ca(NO3)2+Na2CO3
=CaCO3? , Ca(NO3)2+Na2CO3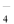 →MnO2 B.ClO3-→Cl-
→MnO2 B.ClO3-→Cl-