题目内容
(1)0.5mol H2O中含有 个水分子.
(2)标准状况下4.48LNH3与 g硫酸所含的分子数相等,它们所含氢原子数之比是 .
(3)含0.4mol Al3+的Al2(SO4)3中所含的S
的物质的量是 .
(2)标准状况下4.48LNH3与
(3)含0.4mol Al3+的Al2(SO4)3中所含的S
| O | 2- 4 |
考点:物质分子中的原子个数计算,阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)根据阿伏伽德罗常数与物质的量的关系计算出含有的分子数;
(2)分子数相同,则含有的物质的量相等,据此计算出硫酸的物质的量及质量;根据氨气与硫酸的物质的量相等及分子中含有的氢原子数目计算出氢原子数之比;
(3)根据硫酸铝的化学式中铝离子与硫酸根离子的关系计算出硫酸根离子的物质的量.
(2)分子数相同,则含有的物质的量相等,据此计算出硫酸的物质的量及质量;根据氨气与硫酸的物质的量相等及分子中含有的氢原子数目计算出氢原子数之比;
(3)根据硫酸铝的化学式中铝离子与硫酸根离子的关系计算出硫酸根离子的物质的量.
解答:
解:(1)0.5mol水中含有的水分子数目为:N(H2O)=0.5mol×NA/mol=0.5NA,
故答案为:0.5NA;
(2)标准状况下4.48LNH3的物质的量为0.2mol,硫酸与氨气的分子数相等,则二者的物质的量相等,0.2mol硫酸的质量为:98g/mol×0.2mol=19.6g;等物质的量的氨气和硫酸中含有的氢原子数目之比等于各自分子中含有的氢原子之比,即:3:2,
故答案为:19.6;3:2;
(3)硫酸铝中铝离子与硫酸根离子物质的量之比为:2:3,含0.4mol Al3+的Al2(SO4)3中所含的硫酸根离子的物质的量为:2:3=0.4mol:n,解得n=0.6mol,
故答案为:0.6 mol.
故答案为:0.5NA;
(2)标准状况下4.48LNH3的物质的量为0.2mol,硫酸与氨气的分子数相等,则二者的物质的量相等,0.2mol硫酸的质量为:98g/mol×0.2mol=19.6g;等物质的量的氨气和硫酸中含有的氢原子数目之比等于各自分子中含有的氢原子之比,即:3:2,
故答案为:19.6;3:2;
(3)硫酸铝中铝离子与硫酸根离子物质的量之比为:2:3,含0.4mol Al3+的Al2(SO4)3中所含的硫酸根离子的物质的量为:2:3=0.4mol:n,解得n=0.6mol,
故答案为:0.6 mol.
点评:本题考查了有关物质的量的计算,题目难度中等,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的转化关系,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
短周期主族元素X、Y、Z、W的原子序数依次增大,X与Y的最外层电子数之比为4:5,X的最高正价是Z的最低负价的绝对值的两倍.Z的原子半径大于Y的原子半径.下列说法正确的是( )
| A、Y的最简单气态氢化物的水溶液呈酸性 |
| B、X的氢化物中一定含有极性共价键,也可能含有非极性共价键 |
| C、标准状况下,等质量Z的两个氧化物,其体积之比为5:4 |
| D、X与W形成的化合物中混有一定量的水,最好采用蒸馏方法分离 |
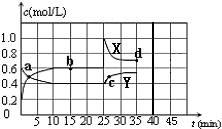 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.请回答:
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.请回答: