题目内容
下列化学反应的离子方程式正确的是( )
| A、将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| B、向氢氧化钠溶液中通入少量CO2:CO2+OH-=HCO3- |
| C、铝片放入NaOH溶液中:2OH-+Al=AlO2-+H2↑ |
| D、往碳酸钙中滴加稀盐酸:CO32-+2H+=CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.不遵循电荷守恒定律;
B.反应生成碳酸钠和水;
C.铝能和烧碱反应产生氢气和偏铝酸钠;
D.碳酸钙在离子反应中保留化学式.
B.反应生成碳酸钠和水;
C.铝能和烧碱反应产生氢气和偏铝酸钠;
D.碳酸钙在离子反应中保留化学式.
解答:
解:A.方程式左边带2个单位的正电荷,右边带3个单位的正电荷,铜屑中加入足量氯化铁溶液,正确的离子方程式为2Fe3++Cu=2Fe2++Cu2+,故A正确;
B.向氢氧化钠溶液中通入少量CO2:CO2+2OH-=CO32-+H2O,故B错误;
C.铝和烧碱反应的实质是:2Al+2OH-+2H2O=2AlO2-+3H2↑,故C错误;
D.向碳酸钙上滴加稀盐酸的离子反应为2H++CaCO3=CO2↑+H2O+Ca2+,故D错误.
故选A.
B.向氢氧化钠溶液中通入少量CO2:CO2+2OH-=CO32-+H2O,故B错误;
C.铝和烧碱反应的实质是:2Al+2OH-+2H2O=2AlO2-+3H2↑,故C错误;
D.向碳酸钙上滴加稀盐酸的离子反应为2H++CaCO3=CO2↑+H2O+Ca2+,故D错误.
故选A.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意选项B为解答的易错点,题目难度中等.

练习册系列答案
相关题目
某混合液中含有等物质的量的CuSO4、FeSO4、Fe2(SO4)3.已知如表数据,下列叙述正确的是( )
| 物质(25℃) | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 完全沉淀时的pH | ≥6.4 | ≥9.6 | ≥3~4 |
A、混合溶液中:c(SO
| ||
| B、若向混合溶液中加入铁粉,不可能观察到红色固体析出 | ||
| C、若向混合溶液中加入足量氯水,调节pH到3-4后过滤,得到纯净的CuSO4溶液 | ||
| D、若向混合溶液中逐滴加入烧碱溶液,首先生成Fe(0H)3沉淀 |
下列离子方程式不正确的是( )
A、用两个铜电极电解饱和食盐水:2Cl-+2H2O
| ||||
| B、AgCl悬浊液中加入硫化钠饱和溶液:2AgCl+S2-=Ag2S+2Cl- | ||||
| C、氢氧化镁与稀硫酸反应:H++OH-=H2O | ||||
D、向20mL沸水中滴入1mL饱和FeCl3溶液,继续煮沸至溶液呈红褐色:Fe3++3H2O
|
下列有关实验原理、装置、操作或结论的描述中,不正确的是( )
A、 测量一定时间内生成H2的反应速率 |
B、 用CO2做喷泉实验 |
C、 除去Cl2中的少量HCl |
D、 比较Na2CO3与NaHCO3的热稳定性 |
下列离子方程式书写正确的是( )
| A、电解饱和食盐水的阳极反应:2H2O+2e-=H2↑+2OH- | ||
B、碳酸钠溶液呈碱性的原因:CO
| ||
C、向AgNO3溶液中加入过量氨水:Ag++NH3?H2O=AgOH↓+NH
| ||
D、泡沫灭火器反应原理:A12++3HCO
|
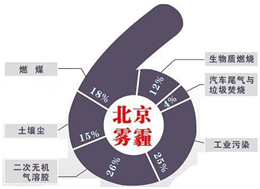 中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5化学组成及来源的季节变化研究发现,北京PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.
中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5化学组成及来源的季节变化研究发现,北京PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.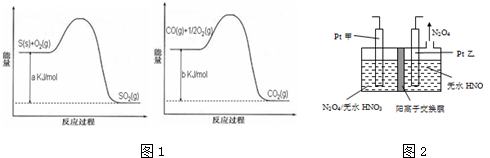

 草酸亚铁(FeC2O4)常用作分析剂、显影剂以及新型电池材料磷酸亚铁锂的生产.
草酸亚铁(FeC2O4)常用作分析剂、显影剂以及新型电池材料磷酸亚铁锂的生产.