题目内容
2.实验室用密度为1.25g/ml,质量分数为36.5%浓盐酸配制250ml0.1mol/L的盐酸溶液,填空并请回答下列问题:(1)配制250ml0.1mol/L的盐酸溶液
| 应量取盐酸体积/ml | 应选用容量瓶的规格/ml | 除容量瓶外还需要的其它仪器 |
A.用30ml水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加少量水(约30ml),用玻璃棒慢慢搅动,使其混合均匀
C.将冷却的盐酸沿玻璃棒注入250ml的容量瓶中
D.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
E.将容量瓶盖紧,振荡,摇匀
F.改用胶头滴管加水,使溶液凹面恰好与刻度相切
(3)操作A中,将洗涤液均注入容量瓶,其目的是防止烧杯中的残留液没有移入容量瓶使溶液浓度减少.溶液注入容量瓶前需恢复到室温,这是因为盐酸溶解放热使溶液体积膨胀,不冷却会使溶液浓度增大..
(4)若实验过程中出现下列情况如何处理?
加蒸馏水时不慎超过了刻度重新配制;向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面重新配制.
分析 (1)依据C=$\frac{1000ρω}{M}$计算浓盐酸的物质的量浓度,依据配制溶液体积选择容量瓶规格,溶液稀释过程中溶质的物质的量不变,据此计算需要浓盐酸的体积;依据配制一定物质的量一般步骤选择需要仪器;
(2)配制一定物质的量浓度溶液的步骤:计算、称量、稀释、冷却、移液、定容、摇匀、装瓶等,据此排序;
(3)移液后烧杯内壁和玻璃棒上沾有溶质,为保证溶质全部转移到容量瓶,应进行洗涤;依据热胀冷缩原理溶液注入容量瓶前不恢复到室温,导致冷却后溶液体积不准确;
(4)不当操作导致实验失败且无法补救的需要重新配制.
解答 解:(1)配制250ml0.1mol/L的盐酸溶液,应选择250mL容量瓶;浓盐酸的物质量浓度为C=$\frac{1000×1.25×36.5%}{36.5}$=12.5mol/L,设需要浓硫酸体积为V,溶液稀释过程中溶质的物质的量不变则:V×12.5mol/L=250mL×0.1mol/L,解得V=2.0mL;
配制溶液的操作步骤:首先计算出需要的溶质的质量(浓硫酸体积),然后天平称量(量筒量取),后放入烧杯中溶解(稀释),同时用玻璃棒搅拌,待溶液冷却至室温后,用玻璃杯引流移液至250ml容量瓶,然后洗涤烧杯和玻璃棒2至3次,将洗涤液也注入容量瓶,然后向容量瓶中注水,至液面离刻度线1至2CM时,改用胶头滴管逐滴加入,至凹液面与刻度线相切,然后摇匀、装瓶.在此过程中用到的仪器有:量筒、烧杯、玻璃棒、250ml容量瓶、胶头滴管,除容量瓶外还需要的其它仪器:烧杯、玻璃棒、量筒、胶头滴管;
故答案为:2.0;250ml;烧杯、玻璃棒、量筒、胶头滴管;
(2)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀装瓶贴标签,所以正确的步骤为:BCADFE;
故答案为:BCADFE;
(3)移液后烧杯内壁和玻璃棒上沾有溶质,为保证溶质全部转移到容量瓶,应进行洗涤,如果不洗涤烧杯中的残留液没有移入容量瓶使溶液浓度减少;依据热胀冷缩原理:盐酸溶解放热使溶液体积膨胀,不冷却会使溶液浓度增大;
故答案为:防止烧杯中的残留液没有移入容量瓶使溶液浓度减少;盐酸溶解放热使溶液体积膨胀,不冷却会使溶液浓度增大;
(4)加蒸馏水时不慎超过了刻度,导致实验失败且不能补救,所以需要重新配制;
向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,导致溶质损耗,实验失败且不能补救,所以需要重新配制;
故答案为:重新配制;重新配制.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择及使用注意事项,题目难度不大.

| A. | 使用食品添加剂与提倡绿色食品相违背 | |
| B. | 含有食品添加剂的食品应该少食,以防中毒 | |
| C. | 没有加任何添加剂的天然食品是最安全的 | |
| D. | 食品添加剂在合理限量范围内不影响人体健康 |
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(2)250s时,H2的转化率为30%.
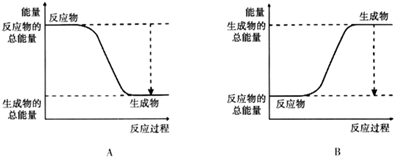
(3)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化92 kJ.下图能正确表示该反应中能量变化的是A.
(4)为加快反应速率,可以采取的措施b
a.降低温度 b.增大压强 c.恒容时充入He气d.恒压时充入He气 e.及时分离NH3
(5)下列说法错误的是d
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.为了提高N2的转化率,应适当提高H2的浓度
d.250~350s生成物浓度保持不变,反应停止.
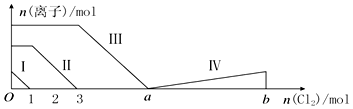
| A. | 线段Ⅱ表示Br-的变化情况 | |
| B. | 线段Ⅳ表示IO3-的变化情况,其中IO3-增加了5moL. | |
| C. | a=6 | |
| D. | 原溶液中n(FeI2):n(FeBr2)=3:1 |
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题.
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题.