题目内容
9.下列叙述错误的是( )| A. | 带相反电荷离子之间的静电作用称为离子键 | |
| B. | 金属元素与非金属元素化合时,不一定形成离子键 | |
| C. | 某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键 | |
| D. | 非金属元素形成的化合物中不可能含有离子键 |
分析 A.阴阳离子之间的相互作用称为离子键;
B.金属元素与非金属元素化合时不一定形成离子键,可能形成共价键;
C.最外层只有一个电子的元素可能为H、Li、Na、K等;
D.铵盐是由非金属元素形成的离子化合物.
解答 解:A.阴阳离子之间的相互作用,即带相反电荷的离子之间的相互作用称为离子键,相互作用包含吸引力、排斥力,故A正确;
B.金属元素与非金属元素化合时不一定形成离子键,可能形成共价键,如AlCl3,故B正确;
C.最外层只有一个电子的元素可能为H、Li、Na、K等,它跟卤素结合时所形成的化学键不一定是离子键,可能是共价键,故C正确;
D.铵盐是由非金属元素形成的离子化合物,所以非金属元素形成的化合物中可能含有离子键,故D错误;
故选D.
点评 本题考查离子键、化合物与化学键的关系等知识点,侧重考查基本概念,注意不能根据是否含有金属元素判断离子键,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
4.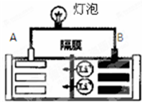 常见的一种锂离子电池的工作原理为LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6.电池工作时如图所示.下列说法不正确的是( )
常见的一种锂离子电池的工作原理为LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6.电池工作时如图所示.下列说法不正确的是( )
 常见的一种锂离子电池的工作原理为LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6.电池工作时如图所示.下列说法不正确的是( )
常见的一种锂离子电池的工作原理为LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6.电池工作时如图所示.下列说法不正确的是( )| A. | 该电池放电时A为负极 | |
| B. | 该电池放电时正极的电极反应式为:Li1-xCoO2+xLi+xe?═LiCoO2 | |
| C. | 该电池充电时阳极质量减轻 | |
| D. | 该电池充电时阴极的电极反应式为:6C+xLi++xe-═LixC6 |
14.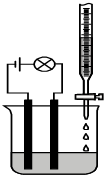 某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
请根据上述题意,回答下列问题:
(1)可观察到的现象为灯泡由亮到暗到灭再到亮,溶液中有白色沉淀产生;当15.0ml 0.10mol/L Ba(OH)2溶液全部滴入H2SO4溶液中后,反应的离子方程式SO42-+2H++Ba2++2OH-═BaSO4↓+2H2O.
(2)有关该实验现象的说法正确的是A
A.溶液的导电性与溶液中自由移动的离子浓度有关
B.灯泡最暗时溶液中自由移动离子的浓度为零
C.往盐酸和硫酸溶液中滴加氢氧化钡溶液时现象相同.
(3)下列物质是该实验中的反应物和生成物,其中属于弱电解质的是D
A.H2SO4 B.Ba(OH)2 C.BaSO4 D.H2O.
 某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:| Ba(OH)2(ml) | 溶液中的总离子浓度(mol/L) |
| 0.0 | 0.30 |
| 5.0 | 0.10 |
| 10.0 | ≈0.00 |
| 15.0 | 0.06 |
(1)可观察到的现象为灯泡由亮到暗到灭再到亮,溶液中有白色沉淀产生;当15.0ml 0.10mol/L Ba(OH)2溶液全部滴入H2SO4溶液中后,反应的离子方程式SO42-+2H++Ba2++2OH-═BaSO4↓+2H2O.
(2)有关该实验现象的说法正确的是A
A.溶液的导电性与溶液中自由移动的离子浓度有关
B.灯泡最暗时溶液中自由移动离子的浓度为零
C.往盐酸和硫酸溶液中滴加氢氧化钡溶液时现象相同.
(3)下列物质是该实验中的反应物和生成物,其中属于弱电解质的是D
A.H2SO4 B.Ba(OH)2 C.BaSO4 D.H2O.
1.下列离子方程式正确的是( )
| A. | HCO3-+H2O?H2CO3+OH- | B. | Al3++3H2O?Al(OH)3+3H+ | ||
| C. | 2Al3++3CO32-?Al2(CO3)3 | D. | Br-+H2O?HBr+OH- |
18.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kur Wuethrich等人为此获得2002年度诺贝尔化学奖.下面叙述正确的是( )
| A. | 15N与14N互为同位素 | |
| B. | 13C与C60互为同素异形体 | |
| C. | 13C和15N的质量数相等,中子数也相等 | |
| D. | 15N的核外电子数与中子数相同 |