题目内容
 已知1,2二氯乙烷常温下为无色液体,沸点83.5℃,密度1.23g/mL,难溶于水,易溶于醇、醚、丙酮等有机溶剂.乙醇的沸点为78.5℃.某化学课外活动小组为探究1,2二氯乙烷的消去反应,设计了如下实验装置.请回答下列问题.
已知1,2二氯乙烷常温下为无色液体,沸点83.5℃,密度1.23g/mL,难溶于水,易溶于醇、醚、丙酮等有机溶剂.乙醇的沸点为78.5℃.某化学课外活动小组为探究1,2二氯乙烷的消去反应,设计了如下实验装置.请回答下列问题.(1)请回答如何检查装置气密性
(2)向装置A中大试管里先加入1,2二氯乙烷和NaOH的乙醇溶液,再加入碎瓷片,目的是
(3)为了使反应在75℃左右进行,常用的方法是
(4)与装置A中大试管相连接的长玻璃管的作用是
(5)证明1,2二氯乙烷已发生消去反应的现象是
考点:性质实验方案的设计
专题:
分析:(1)化学实验装置的气密性检验的原理是使装置内外的压强不相等,基本方法是观察气泡或液面变化;
(2)根据题干信息,反应物的沸点低需加沸石防止暴沸;
(3)用酒精灯的外焰给试管底部加热时温度太高,反应在75℃左右进行,应水浴加热;
(4)与装置A中大试管相连接的长玻璃管除了起导气的作用,还起到了冷凝回流的作用;装置B的作用防止倒吸;
(5)根据氯代烃在氢氧化钠醇溶液中能发生消去反应,生成含有不饱和键的有机物易与溴发生加成反应分析解答;
(2)根据题干信息,反应物的沸点低需加沸石防止暴沸;
(3)用酒精灯的外焰给试管底部加热时温度太高,反应在75℃左右进行,应水浴加热;
(4)与装置A中大试管相连接的长玻璃管除了起导气的作用,还起到了冷凝回流的作用;装置B的作用防止倒吸;
(5)根据氯代烃在氢氧化钠醇溶液中能发生消去反应,生成含有不饱和键的有机物易与溴发生加成反应分析解答;
解答:
解:(1)设法使装置内外形成气压差是气密性检查的常用手段,在连接好装置后,将导气管末端插入盛水的烧杯中,用酒精灯加热(或用手捂)装置A中大试管,气体受热体积膨胀,若导气管末端有气泡出现,且移开酒精灯(或松开手)一会儿,导气管中出现一段水柱,则证明不漏气,
故答案为:将导气管末端插入盛水的烧杯中,用酒精灯加热(或用手捂)装置A中大试管,若导气管末端有气泡出现,且移开酒精灯(或松开手)一会儿,导气管中出现一段水柱,则证明不漏气;
(2)1,2二氯乙烷常温下为无色液体,沸点83.5℃,乙醇的沸点为78.5℃,1,2二氯乙烷和NaOH的乙醇溶液反应,因反应物沸点低,为防止暴沸,需加沸石,
故答案为:防止暴沸;
(3)因为水的沸点是100℃,用水浴加热的温度不可能超过100℃,水浴加热的温度是使反应容器内试剂受热温度均匀,便于控制反应的温度,为了使反应在75℃左右进行,常用的方法是将装置A中大试管放在75℃左右的水浴中加热,
故答案为:将装置A中大试管放在75℃左右的水浴中加热;
(4)A装置中1,2-二氯乙烷、乙醇沸点低,易挥发,与装置A中大试管相连接的长玻璃管除了起导气的作用,还起到了冷凝回流的作用,装置A中发生消去反应生成含有不饱和键的有机物易与溴发生加成反应,装置B能防止C中的液体倒流到A中,起缓冲防倒吸的作用,
故答案为:冷凝、回流;防止倒吸;
(5)1,2二氯乙烷已发生消去反应,生成含有不饱和键的有机物易与溴发生加成反应,溴水褪色;
装置A中:1,2-二氯乙烷在氢氧化钠醇溶液中能发生消去反应,生成氯烯烃、氯化钠和水,方程式为:CH2ClCH2Cl+NaOH
CHCl=CH2↑+NaCl+H2O或CH2ClCH2Cl+2NaOH
CH≡CH↑+2NaCl+2H2O,
装置C中:氯乙烯含有碳碳双键,可与溴水发生加成反应,溴水褪色,反应的方程式为CHCl=CH2+Br2→CHClBrCH2Br或CH≡CH+Br2→CHBr═CHBr或CH≡CH+2Br2→CHBr2CHBr2,
故答案为:溴水褪色;CH2ClCH2Cl+NaOH
CHCl=CH2↑+NaCl+H2O或CH2ClCH2Cl+2NaOH
CH≡CH↑+2NaCl+2H2O;CHCl=CH2+Br2→CHClBrCH2Br或CH≡CH+Br2→CHBr═CHBr或CH≡CH+2Br2→CHBr2CHBr2;
故答案为:将导气管末端插入盛水的烧杯中,用酒精灯加热(或用手捂)装置A中大试管,若导气管末端有气泡出现,且移开酒精灯(或松开手)一会儿,导气管中出现一段水柱,则证明不漏气;
(2)1,2二氯乙烷常温下为无色液体,沸点83.5℃,乙醇的沸点为78.5℃,1,2二氯乙烷和NaOH的乙醇溶液反应,因反应物沸点低,为防止暴沸,需加沸石,
故答案为:防止暴沸;
(3)因为水的沸点是100℃,用水浴加热的温度不可能超过100℃,水浴加热的温度是使反应容器内试剂受热温度均匀,便于控制反应的温度,为了使反应在75℃左右进行,常用的方法是将装置A中大试管放在75℃左右的水浴中加热,
故答案为:将装置A中大试管放在75℃左右的水浴中加热;
(4)A装置中1,2-二氯乙烷、乙醇沸点低,易挥发,与装置A中大试管相连接的长玻璃管除了起导气的作用,还起到了冷凝回流的作用,装置A中发生消去反应生成含有不饱和键的有机物易与溴发生加成反应,装置B能防止C中的液体倒流到A中,起缓冲防倒吸的作用,
故答案为:冷凝、回流;防止倒吸;
(5)1,2二氯乙烷已发生消去反应,生成含有不饱和键的有机物易与溴发生加成反应,溴水褪色;
装置A中:1,2-二氯乙烷在氢氧化钠醇溶液中能发生消去反应,生成氯烯烃、氯化钠和水,方程式为:CH2ClCH2Cl+NaOH
| 乙醇 |
| △ |
| 乙醇 |
| △ |
装置C中:氯乙烯含有碳碳双键,可与溴水发生加成反应,溴水褪色,反应的方程式为CHCl=CH2+Br2→CHClBrCH2Br或CH≡CH+Br2→CHBr═CHBr或CH≡CH+2Br2→CHBr2CHBr2,
故答案为:溴水褪色;CH2ClCH2Cl+NaOH
| 乙醇 |
| △ |
| 乙醇 |
| △ |
点评:本题主要考查了氯代烃的性质,侧重考查了氯代烃在氢氧化钠醇溶液中能发生消去反应、有机化学方程式的书写,熟悉反应物的结构和性质是解题的关键,题目难度中等.

练习册系列答案
相关题目
下列对实验现象的解释与结论正确的是( )
| A、除去SO2中少量HCl的方法是:将混合气体通过盛有NaHSO3饱和溶液的洗气瓶 |
| B、用蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口,有大量白烟,说明该无机酸一定为盐酸 |
| C、向铜和稀硫酸的混合物中加入无色溶液,溶液逐渐变成蓝色,铜逐渐溶解,则该无色溶液一定是硝酸 |
| D、向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
下列有关实验原理或实验操作结论正确的是( )
| A、配制酸性KMnO4溶液时,用盐酸酸化 |
| B、用水湿润pH试纸测量某溶液的pH值 |
C、实验室用右图所示装置除去Cl2中的少量HCl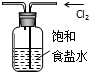 |
| D、用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
一定温度下,下列溶液的离子浓度关系式正确的是( )
| A、pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③ | ||
| B、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol?L-1 | ||
| C、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | ||
D、pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O
|