题目内容
19.有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32-?CaCO3(s)+SO42-.已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字).
分析 以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq)平衡常数概念写出计算式,依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算分析.
解答 解:溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq),CaCO3(s)=Ca2++CO32-、CaSO4(s)=Ca2++SO42-,
依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同可知,反应CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq)的平衡常数为:K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=$\frac{{K}_{sp}(CaS{O}_{4})}{{K}_{sp}(CaC{O}_{3})}$=$\frac{4.90×1{0}^{-5}}{2.80×1{0}^{-9}}$=1.75×104,
答:此温度下该反应的平衡常数为1.75×104.
点评 本题考查了难溶物溶解平衡及其应用,题目难度中等,明确难溶物溶解平衡的影响因素为解答关键,注意掌握溶度积的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
(1)11种元素中,化学性质最不活泼的是Ar.
(2)①②⑤中,最高价氧化物的水化物,碱性最强的物质化学式为KOH.
(3)①③⑦⑪中形成的简单离子半径由大到小的顺序是O2->F->Na+>Mg2+.
(4)元素⑦的氢化物分子式为H2O,用电子式表示该物质的形成过程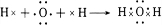 .
.
(5)⑧的最高价氧化物对应的水化物化学式为HClO4.①和⑨两元素形成化合物的化学式为NaBr,该化合物灼烧时焰色为黄色,该化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤中,最高价氧化物的水化物,碱性最强的物质化学式为KOH.
(3)①③⑦⑪中形成的简单离子半径由大到小的顺序是O2->F->Na+>Mg2+.
(4)元素⑦的氢化物分子式为H2O,用电子式表示该物质的形成过程
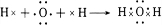 .
.(5)⑧的最高价氧化物对应的水化物化学式为HClO4.①和⑨两元素形成化合物的化学式为NaBr,该化合物灼烧时焰色为黄色,该化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
4.下列离子方程式正确的是( )
| A. | 铝溶于NaOH溶液:Al+2OH-═AlO2-+H2↑ | |
| B. | 稀硫酸中滴加氢氧化钡溶液:H++OH-═H2O | |
| C. | 碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| D. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu |
11.如图所示的装置最适宜于收集的气体是( )
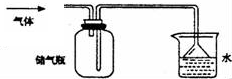

| A. | HCl | B. | NH3 | C. | NO | D. | NO2 |
8.下列有关同分异构体数目的叙述中,正确的是( )
| A. | 碳原子数小于或等于10的烷烃中其一氯代物只有一种的烷烃有4种 | |
| B. | C8H10中只有三种属于芳香烃的同分异构体 | |
| C. | 结构简式为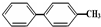 的烃,分子中含有两个苯环的该烃的同分异构体为4种 的烃,分子中含有两个苯环的该烃的同分异构体为4种 | |
| D. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种 |
3. 某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)关于催化剂在化学反应中的作用,下列叙述正确的是AD(填字母).
A.使反应活化能降低 B.使反应焓变减小 C.使平衡常数增大 D.使反应速率加快
(2)实验①和②的目的是探究反应物浓度对反应速率的影响.实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是:向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中).
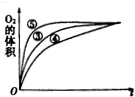
(3)实验③④⑤中,测得生成O2的体积随时间变化关系如图.分析该图可得出的结论是:碱性环境可加快反应速率;酸性环境可减慢反应速率.
 某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2的分解为例,研究反应物浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 分 组 实 验 | 催化剂 | |
| ① | 10mL 5%的H2O2溶液 | 无 |
| ② | 10mL 2%的H2O2溶液 | 无 |
| ③ | 10mL 5%的H2O2溶液 | 1mL 0.1mol/L的FeCl3溶液 |
| ④ | 10mL 5%的H2O2溶液+少量盐酸 | 1mL 0.1mol/L的FeCl3溶液 |
| ⑤ | 10mL 5%的H2O2溶液+少量NaOH溶液 | 1mL 0.1mol/L的FeCl3溶液 |
A.使反应活化能降低 B.使反应焓变减小 C.使平衡常数增大 D.使反应速率加快
(2)实验①和②的目的是探究反应物浓度对反应速率的影响.实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是:向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中).
(3)实验③④⑤中,测得生成O2的体积随时间变化关系如图.分析该图可得出的结论是:碱性环境可加快反应速率;酸性环境可减慢反应速率.