题目内容
14.研究电化学腐蚀及防护的装置如图所示.下列有关说法正确的是( )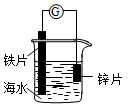
| A. | 锌片发生氧化反应作阴极 | |
| B. | 电子从铁片经过导线流向锌片 | |
| C. | 铁片上电极反应为:O2+2H2O+4e→4OH- | |
| D. | 该装置可用于研究外加电流阴极保护法 |
分析 A、锌比铁片活泼,所以腐蚀锌;
B、电子从负极沿导线流向正极;
C、铁为正极,发生吸氧腐蚀;
D、该装置可用于研究牺牲阳极的阴极保护法.
解答 解:A、锌比铁片活泼,所以腐蚀锌,锌是负极,而不是阴极,故A错误;
B、电子从负极沿导线流向正极,所以电子从锌片经过导线流向铁片,故B错误;
C、铁为正极,发生吸氧腐蚀,电极反应式为O2+2H2O+4e-=4OH-,故C正确;
D、该装置可用于研究牺牲阳极的阴极保护法,而不是用于研究外加电流阴极保护法,故D错误;
故选C.
点评 本题考查了原电池原理,根据电极上得失电子判断正负极,再结合电极反应类型来分析解答,熟记原电池原理,难点是电极反应式的书写.

练习册系列答案
相关题目
4.电化学在日常生活中用途广泛,图甲是镁--次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理.下列说法正确的是( )
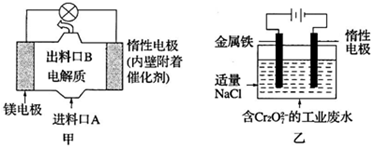

| A. | 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 | |
| B. | 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ | |
| C. | 图乙电解池中,若有0.84g阳极材料参与反应,则阴极会有3.36L的气体产生 | |
| D. | 若图甲燃料电池消耗0.36g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀 |
2.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 电解精炼铜,当外电路通过NA个电子时;阳极质量减少32 g | |
| B. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92kJ•mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA | |
| C. | lmol•L1的氯化铜溶液中,若Cl-的数目为2Na,则Cu2+的数目为NA | |
| D. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA |
9.X、Y、M、N是四种短周期主族元素,原子序数依次增大.X与M同主族,M原子的最外层电子数是内层电子数的一半,四种元素原子最外层电子数之和为19,N的单质是一种有色气体,可用于自来水的消毒.下列说法正确的是( )
| A. | 原子半径:r(N)>r(M)>r(Y)>r(X) | |
| B. | X与Y形成的化合物溶于水,溶液显碱性 | |
| C. | 简单气态氢化物的热稳定性:M>N>X | |
| D. | 单质的熔点:Y>N>M>X |
19.工业上常用NaHSO3处理含Cr2O72-的废液,反应的离子方程式为:5H++Cr2O72-+3HSO3-→2Cr3++3SO42-+4H2O
下列判断错误的是( )
下列判断错误的是( )
| A. | 氧化产物是SO42- | |
| B. | 氧化剂与还原剂的物质的量之比是1:3 | |
| C. | Cr2O72-表现了氧化性 | |
| D. | 还原1molCr2O72-,电子转移3mol |
6.下列有关实验操作、现象和结论都正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向稀硝酸中加入过量的铁粉充分反应后,滴入KSCN溶液 | 溶液变为血红色 | HNO3具有氧化性,能将Fe氧化成Fe3+ |
| B | 向盛有某溶液的试管中滴加NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无NH4+ |
| C | 向淀粉溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2,再加热 | 未见红色沉淀 | 淀粉未发生水解 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
3.设NA表示阿伏加德罗的数值.下列说法正确的是 ( )
| A. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| B. | 0.1mol•L-1(NH4)2SO4溶液与0.2mol•L-1NH4Cl溶液中的NH4+数目相同 | |
| C. | H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA | |
| D. | 含0.1molNH4HSO4的溶液中,阳离子数目略大于0.21NA |
14.某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、Zn2+、CO32-、SO42-,现取两份溶液各100mL分别进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生
根据上述实验,以下有关原溶液的论断不正确的是( )
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生
根据上述实验,以下有关原溶液的论断不正确的是( )
| A. | Cl-一定存在 | |
| B. | CO32-和SO42-一定存在,且二者的个数比为1:2 | |
| C. | Zn2+和Ca2+一定不存在 | |
| D. | 100mL溶液中K+的质量不小于2.34g |