题目内容
铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2?2H2O),为制取纯净的CuCl2?2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
请回答下列问题:
(1)得到溶液Ⅱ,需加入氧化剂X,最适合作氧化剂X的是 .
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂X的目的是 .
(3)为了除去Fe3+,需加入物质Y调节溶液的PH值为
(4)最后能不能直接蒸发结晶得到CuCl2?2H2O晶体? (填“能”或“不能”).若能,不用回答;若不能,回答该如何操作? .
(5)已知Fe(OH)3的Ksp=1×10-35mol4/L4;若Fe3+沉淀完全时,在溶液中Fe3+的浓度为1×10-5mol/L,则此时溶液的PH最小为 .

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
(1)得到溶液Ⅱ,需加入氧化剂X,最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂X的目的是
(3)为了除去Fe3+,需加入物质Y调节溶液的PH值为
(4)最后能不能直接蒸发结晶得到CuCl2?2H2O晶体?
(5)已知Fe(OH)3的Ksp=1×10-35mol4/L4;若Fe3+沉淀完全时,在溶液中Fe3+的浓度为1×10-5mol/L,则此时溶液的PH最小为
考点:物质分离和提纯的方法和基本操作综合应用,难溶电解质的溶解平衡及沉淀转化的本质
专题:实验设计题
分析:氯化亚铁和氯化铜的混合液中,加入氧化剂可以将亚铁离子氧化为铁离子,调节pH可以将铁离子沉淀,得到氯化铜的水溶液,然后再酸性环境下蒸发浓缩、冷却结晶,过滤、洗涤、干燥即可得到氯化铜晶体,
(1)选择的氧化剂不能引进新的杂质离子是最佳氧化剂;
(2)加入氧化剂,将Fe2+氧化为Fe3+,易除去;
(3)为了除去Fe3+,在调节pH时,注意不能生成氢氧化铜沉淀;
(4)铜离子水解溶液显示酸性,加热蒸干硫酸铜溶液得到的是氢氧化铜;
(5)Fe3+的浓度为1×10-5mol/L,结合Fe(OH)3的Ksp=1×10-35mol4/L4计算.
(1)选择的氧化剂不能引进新的杂质离子是最佳氧化剂;
(2)加入氧化剂,将Fe2+氧化为Fe3+,易除去;
(3)为了除去Fe3+,在调节pH时,注意不能生成氢氧化铜沉淀;
(4)铜离子水解溶液显示酸性,加热蒸干硫酸铜溶液得到的是氢氧化铜;
(5)Fe3+的浓度为1×10-5mol/L,结合Fe(OH)3的Ksp=1×10-35mol4/L4计算.
解答:
解:氯化亚铁和氯化铜的混合液中,加入氧化剂可以将亚铁离子氧化为铁离子,调节pH可以将铁离子沉淀,得到氯化铜的水溶液,然后再酸性环境下蒸发浓缩、冷却结晶,过滤、洗涤、干燥即可得到氯化铜晶体,
(1)根据框图,加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为H2O2,故答案为:C;
(2)Fe2+沉淀为氢氧化物时所需pH与Cu2+的沉淀的pH相同,也就是说,Fe2+沉淀的同时,Cu2+也会沉淀,无法将两者分离开,根据题干提供信息可知Fe3+沉淀所需的pH较小,所以应先将Fe2+氧化为Fe3+后再将其除去,
故答案为:将Fe2+氧化成Fe3+,便于生成Fe(OH)3沉淀而与Cu2+分离;
(3)结合题示,调节pH3.2~4.7,使Fe3+全部沉淀,故答案为:3.2-4.7之间;
(4)CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),所以应在HCl或SOCl2等混合液气氛中采用加热蒸发结晶的方法,以得到CuCl2?2H2O的晶体,
故答案为:不能;应在HCl气流中加热蒸发结晶;
(5)Fe(OH)3的Ksp=1×10-35mol/L,当铁离子沉淀完全时,c(OH-)=
=1×10-10mol/L,则c(H+)=1×10-4mol/L,pH=4,
故答案为:4.
(1)根据框图,加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为H2O2,故答案为:C;
(2)Fe2+沉淀为氢氧化物时所需pH与Cu2+的沉淀的pH相同,也就是说,Fe2+沉淀的同时,Cu2+也会沉淀,无法将两者分离开,根据题干提供信息可知Fe3+沉淀所需的pH较小,所以应先将Fe2+氧化为Fe3+后再将其除去,
故答案为:将Fe2+氧化成Fe3+,便于生成Fe(OH)3沉淀而与Cu2+分离;
(3)结合题示,调节pH3.2~4.7,使Fe3+全部沉淀,故答案为:3.2-4.7之间;
(4)CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),所以应在HCl或SOCl2等混合液气氛中采用加热蒸发结晶的方法,以得到CuCl2?2H2O的晶体,
故答案为:不能;应在HCl气流中加热蒸发结晶;
(5)Fe(OH)3的Ksp=1×10-35mol/L,当铁离子沉淀完全时,c(OH-)=
| 3 |
| ||
故答案为:4.
点评:本题综合考查物质的分离和提纯,为高频考点,侧重于学生的分析能力和计算能力的考查,题目考查的知识点较多,涉及氧化还原反应原理的应用、调节pH除杂质、盐的水解原理的应用等,有利于培养学生分析解决问题以及灵活应用所学知识的能力,题目难度中等.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
下列做法与化学反应速率无关的是( )
| A、延长反应时间 |
| B、使用合适的催化剂 |
| C、增加反应物的浓度 |
| D、改变反应的温度 |
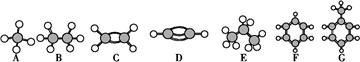
下列化合物的分子中,所有C原子都处于同一平面的有( )
①丙烷 ②乙苯 ③异丁烷 ④溴苯.
①丙烷 ②乙苯 ③异丁烷 ④溴苯.
| A、①② | B、②③ | C、③④ | D、①④ |
有机化合物C4H8是生活中的重要物质,下列关于C4H8的说法中错误的是( )
| A、C4H8可能是烯烃 |
| B、C4H8中属于烯烃类的同分异构体有4种 |
C、核磁共振氢谱有2种吸收峰的烯烃结构一定是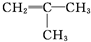 |
| D、C4H8中属于烯烃的顺反异构体有2种 |
 在容积为2L的密闭容器中,进行如下反应:
在容积为2L的密闭容器中,进行如下反应:


 25℃时,已知某些物质的电离平衡常数如表:
25℃时,已知某些物质的电离平衡常数如表: