题目内容
10.A、B、C是单质,其中A是金属,各种物质间的转化关系如图:根据图示转化关系回答:

(1)写出下列物质的化学式. AAl,乙NaAlO2.
(2)写出下列变化的化学方程式.
①A与NaOH溶液反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
②甲与NaOH溶液反应的化学方程式Al2O3+2OH-═2AlO2-+H2O.
③乙通入过量CO2反应的离子方程式AlO2-+CO2+2H2O=Al(OH)3+HCO3-.
(3)将一定量的A加 入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为0.1mol,转移电子的物质的量为0.3mol.
分析 常见金属单质中能与NaOH溶液反应产生气体的只有Al,所以A是Al,乙是NaAlO2,C是H2;甲是Al的化合物,可和NaOH溶液反应产生NaAlO2,可甲能是Al2O3,则丙是H2O,B即是O2,根据NaAlO2+CO2+2H2O═NaHCO3+Al(OH)3↓得丁是Al(OH)3,验证符合转化关系,以此解答该题.
解答 解:(1)由上述分析可知,乙是NaAlO2,A为Al,
故答案为:Al;NaAlO2;
(2)①Al与NaOH溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2 O═2NaAlO2+3H2↑;
②Al2O3与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
③乙溶液中通入过量CO2反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3+HCO3-;
(3)产生的H2在标准状况下的体积为3.36L,物质的量为$\frac{3.36L}{22.4L/mol}$=0.15mol,根据2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,消耗的Al的物质的量为0.15mol×$\frac{2}{3}$=0.1mol,转移电子的物质的量为0.1mol×3=0.3mol,
故答案为:0.1 mol;0.3 mol.
点评 本题以“无机框图题”的形式考查元素单质及其化合物的性质,为高考常见题型,涉及化学式及离子方程式书写等,难度中等,在熟练掌握元素化合物知识的基础上着重考查学生的发散思维、分析判断、逻辑思维以及对无机物知识的综合应用等能力,Al与碱的特殊的反应是推断的关键.

| A. | 无色溶液:Ca2+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| C. | 水电离出的c(H+)=10-13mol•L-1的溶液中:K+、Na+、SO42-、ClO- | |
| D. | 有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3- |
| A. | 增大压强 | B. | 升高温度 | ||
| C. | 使用催化剂 | D. | 增加反应物的用量 |
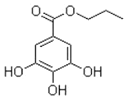 没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )
没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )| A. | 没食子酸丙酯的分子式是 C10Hl3O5 | |
| B. | 1mol没食子酸丙酯能与4mol H2加成 | |
| C. | 1mol没食子酸丙酯能与4mol NaOH反应 | |
| D. | 1mol没食子酸丙酯最多能与3mol浓溴水发生取代反应 |
| A. | 气体最多 | B. | 液体比气体多 | C. | 固体最多 | D. | 以上都不对 |
| A. | 溶液很快褪色,出现沉淀 | B. | 溶液不褪色,不出现沉淀 | ||
| C. | 溶液不褪色,出现沉淀 | D. | 溶液很快褪色,不出现沉淀 |
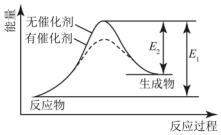
| A. | 该反应为放热反应 | B. | 催化剂改变了化学反应的热效应 | ||
| C. | 催化剂不改变化学反应历程 | D. | 催化剂改变了化学反应历程 |
| A. | 1 mol H2SO4与1 mol Ba(OH)2反应时放出的热叫做中和热 | |
| B. | 500℃、30MPa下,将0.5mol N2和 1.5molH2置于密闭的容器中充分反应生成NH3,放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g);△H=-38.6kJ•mol-1 | |
| C. | Ba(OH)2•8H2O与NH4Cl反应是氧化还原反应,且反应的焓变大于零 | |
| D. | 热化学方程式中的化学计量数表示物质的量,可以是分数 |
C(s)+H2O(g)=CO(g)+H2(g);△H=+131kJ•mol-1
2CO(g)+O2(g)=2CO2(g);△H=-564kJ•mol-1
2H2(g)+O2(g)=2H2O(g);△H=-482kJ•mol-1.
由以上反应推断往炽热的炉膛内通入水蒸气时( )
| A. | 不能节约燃料,但能使炉膛火更旺 | |
| B. | 虽不能使炉膛火更旺,但可节约燃料 | |
| C. | 既可使炉膛火更旺,又能节约燃料 | |
| D. | 既不能使炉膛火更旺,又不能节约燃料 |