题目内容
(12分)【化学——物质结构与性质】铜及其化合物是重要的化工原料。请回答下列问题:
(1)与铜同周期的所有元素的基态原子中,未成对电子数与铜原子相同的元素有 种。Cu+的电子排布式是 。
(2)配离子[Cu(NH3)4(H2O)2]2+含有的微粒间的作用力类型有 ;H、N、O三种元素的第一电离能由大到小的顺序是 。
(3)EDTA( )也可以与铜离子形成配合物。其中碳原子轨道的杂化类型为 。
)也可以与铜离子形成配合物。其中碳原子轨道的杂化类型为 。
(4)CuCl的晶胞结构如图所示,

其中C1-的配位数(即与C1-最近距离的Cu+的个数)为 。
(12分)(1)3种(2分) 1s22s22p63s23p63d10
(2)配位键、极性共价键(2分) N>O>H(2分);(3)sp2、sp3 (2分) (4)4(2分)
【解析】
试题分析:(1)Cu是第四周期的元素,原子的最外层有1个为成对的电子,与铜同周期的所有元素的基态原子中,未成对电子数与铜原子相同的元素有K、Cr、Cu3种。Cu+的电子排布式是1s22s22p63s23p63d10;(2)配离子[Cu(NH3)4(H2O)2]2+含有的微粒间的作用力类型有配位体内的极性共价键、及配位体与Cu2+之间的配位键;一般情况下,元素的非金属性越强,其电负性就越大,但是当原子核外的电子处于白轨道的半充满、全充满或全空时是稳定的状态,失去电子较难,电离能较大,由于N原子核外电子处于其轨道的半充满的稳定状态,失去电子比O还大,所以H、N、O三种元素的第一电离能由大到小的顺序是N>O>H,(3)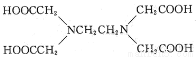 中C原子的杂化方式有sp2、sp3杂化两种方式;(4)在CuCl的晶胞结构中,与Cl-最近的Cu+的个数是4个,与Cu+距离最近的Cl-的个数是4个,即C1-的配位为4。
中C原子的杂化方式有sp2、sp3杂化两种方式;(4)在CuCl的晶胞结构中,与Cl-最近的Cu+的个数是4个,与Cu+距离最近的Cl-的个数是4个,即C1-的配位为4。
考点:考查原子核外电子排布式、络离子的结构、化学键的类型、原子的杂化、元素第一电离能的比较、晶体中微粒的配位数的确定的知识。


 ,有关说法正确的是
,有关说法正确的是 2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

 (Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系: