题目内容
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1.2g金刚石中含有的碳碳单键数为0.4NA |
| B、4.4g二氧化碳中含有的共用电子对数为0.4NA |
| C、常温时11.2L乙烯在氧气中完全燃烧转移的电子数为6.0NA |
| D、常温时0.1mol?L-1硝酸铵溶液中,NH4+和H+总数一定大于0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量结合金刚石中1mol金刚石中含有2molC-C键分析;
B、依据n=
计算物质的量,结合二氧化碳分子结构计算共用电子对数;
C、依据气体摩尔体积条件分析,标准状况气体摩尔体积22.4L/mol;
D、溶液体积不知不能计算微粒数;
| m |
| M |
B、依据n=
| m |
| M |
C、依据气体摩尔体积条件分析,标准状况气体摩尔体积22.4L/mol;
D、溶液体积不知不能计算微粒数;
解答:
解:A、依据n=
计算物质的量=
=0.1mol,结合金刚石中1mol金刚石中含有2molC-C键分析,0.1mol金刚石含有碳碳单键数为0.2NA,故A错误;
B、依据n=
计算物质的量=
=0.1mol,结合二氧化碳分子结构计算共用电子对数=0.1mol×4×NA=0.4NA,故B正确;
C、依据气体摩尔体积条件分析,标准状况气体摩尔体积22.4L/mol,常温时11.2L乙烯物质的量不是0.5mol,故C错误;
D、溶液体积不知不能计算微粒数,故D错误;
故选B.
| m |
| M |
| 1.2g |
| 12g/mol |
B、依据n=
| m |
| M |
| 4.4g |
| 44g/mol |
C、依据气体摩尔体积条件分析,标准状况气体摩尔体积22.4L/mol,常温时11.2L乙烯物质的量不是0.5mol,故C错误;
D、溶液体积不知不能计算微粒数,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,物质结构理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、标准状况下,1mol水的体积是22.4 L |
| B、1mol任何气体,体积均为22.4L |
| C、1mol O2在标准状况下的体积约为22.4L |
| D、标准状况下,气体的摩尔体积是22.4L |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A、CO2的球棍模型示意图: | ||
B、Cl-的结构示意图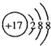 | ||
C、质量数为37的氯原子
| ||
| D、N2的结构式::N≡N: |
丙烯醛的结构是CH2=CH-CHO,下列关于它的性质的叙述中,错误的是( )
| A、能使溴水和高锰酸钾溶液褪色 |
| B、能被新制的氢氧化铜悬浊液氧化 |
| C、在一定条件下,与氢气充分反应生成丙醇 |
| D、能发生银镜反应,体现氧化性 |
1989年世界卫生组织把铝确定为食品污染源之一,而加以控制使用.铝在下列应用时应加以控制的是( )
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水 ⑥明矾与苏打制食品膨松剂 ⑦易拉罐 ⑧用Al(OH)3凝胶制胃舒平药片 ⑨包装糖果和小食品.
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水 ⑥明矾与苏打制食品膨松剂 ⑦易拉罐 ⑧用Al(OH)3凝胶制胃舒平药片 ⑨包装糖果和小食品.
| A、③⑤⑧⑨ | B、③⑤⑥⑦⑧⑨ |
| C、③⑤⑨ | D、⑥⑧⑨ |
下列各种高聚物中,具有热固性的是( )
| A、有机玻璃 | B、聚氯乙烯 |
| C、聚丙烯 | D、酚醛塑料 |
有关Na2CO3 和 NaHCO3的说法正确的是( )
| A、水溶性Na2CO3<NaHCO3 |
| B、二者都能与酸反应生成CO2 |
| C、热稳定性Na2CO3<NaHCO3 |
| D、二者在相同条件下可相互转化 |
 氧化还原反应在生产、生活中具有广泛用途,贯穿古今.
氧化还原反应在生产、生活中具有广泛用途,贯穿古今.