题目内容
下列说法中正确的是( )
| A、NO2、SO2、BF3、NCl3分子没有一个分子中原子的最外层电子都满足了8电子稳定结构 |
| B、P4和CH4都是正四面体分子且键角都为109°28ˊ |
| C、CsCl晶体中与每个Cs+距离相等且最近的Cs+共有6个 |
| D、离子晶体中一定只含有离子键 |
考点:原子核外电子排布,离子化合物的结构特征与性质,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.元素化合价绝对值+元素原子最外层电子数=8,则原子满足8电子结构;
B.P4和CH4都是正四面体分子,P4分子中P原子位于正四面体顶点,CH4分子中C原子位于正四面体中心,H原子位于正四面体的顶点;
C.CsCl晶体中与每个Cs+距离相等且最近的Cs+共有6个;
D.离子晶体可能含有共价键.
B.P4和CH4都是正四面体分子,P4分子中P原子位于正四面体顶点,CH4分子中C原子位于正四面体中心,H原子位于正四面体的顶点;
C.CsCl晶体中与每个Cs+距离相等且最近的Cs+共有6个;
D.离子晶体可能含有共价键.
解答:
解:A.NO2分子中|N元素化合价|+5=9,N原子不满足8电子结构,SO2分子中|S元素化合价|+6=10,S原子不满足8电子结构,BF3分子中|B元素化合价|+3=6,B原子不满足8电子结构,NCl3分子中|N元素化合价|+5=8,|Cl元素化合价|+7=8,N、Cl原子都满足8电子结构,故A错误;
B.P4和CH4都是正四面体分子,CH4分子中C原子位于正四面体中心,H原子位于正四面体的顶点,键角为109°28ˊ,而P4分子中P原子位于正四面体顶点,键角为60°,故B错误;
C.CsCl晶体中每个Cs+周围紧邻的有8个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有6个,故C正确;
D.离子晶体可能含有共价键,如NaOH等,故D错误,
故选C.
B.P4和CH4都是正四面体分子,CH4分子中C原子位于正四面体中心,H原子位于正四面体的顶点,键角为109°28ˊ,而P4分子中P原子位于正四面体顶点,键角为60°,故B错误;
C.CsCl晶体中每个Cs+周围紧邻的有8个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有6个,故C正确;
D.离子晶体可能含有共价键,如NaOH等,故D错误,
故选C.
点评:本题考查分子结构、晶胞结构、化学键等,难度中等,C选项为易错点,注意识记中学常见晶胞结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质所含分子数最少的是( )
| A、标准状况下11.2L HCl |
| B、6.02×1023个N2 |
| C、1.5mol H2O |
| D、32g O2(O2的摩尔质量32g/mol) |
下列反应中,能证明SiO2是酸性氧化物的是( )
| A、SiO2+2C═Si+2CO↑ |
| B、SiO2+2NaOH═Na2SiO3+H2O |
| C、SiO2+4HF═SiF4↑+2H2O |
| D、SiO2+CaCO3═CaSiO3+CO2↑ |
结构为  的有机物可以通过不同的反应得到下列四种物质
的有机物可以通过不同的反应得到下列四种物质

生成这四种有机物的反应类型依次为( )
 的有机物可以通过不同的反应得到下列四种物质
的有机物可以通过不同的反应得到下列四种物质
生成这四种有机物的反应类型依次为( )
| A、取代反应、消去反应、酯化反应、加成反应 |
| B、取代反应、消去反应、加聚反应、取代反应 |
| C、酯化反应、取代反应、缩聚反应、取代反应 |
| D、酯化反应、消去反应、取代反应、氧化反应 |
下列关于复合材料的说法正确的是( )
| A、将不同性质的材料经简单混合便成复合材料 |
| B、合金就是复合材料 |
| C、复合材料中的各部分作用相同 |
| D、复合材料由两种或两种以上不同性质的材料经特殊加工而制成的 |
湖南省质量技术监督局在某酒样品中检出塑化剂邻苯二甲酸二丁酯.邻苯二甲酸二丁酯的结构简式如图所示,该物质在一定条件下不能发生的反应类型是( )
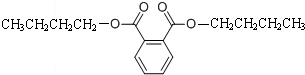

| A、与氯气的取代反应 |
| B、与氢气的加成反应 |
| C、水解反应 |
| D、被新制Cu(OH)2悬浊液氧化的反应 |
由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的是( )
A、 溶解 |
B、 过滤 |
C、 蒸发 |
D、 焰色反应 |