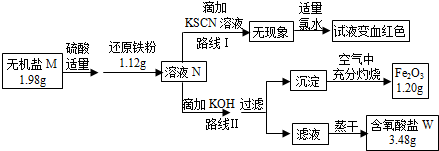
题目内容
19.(1)管道工人曾用浓氨水检验氯气管道是否漏气.发生的反应如下:8NH3+3Cl2=N2+6NH4C1在上述反应中用单线桥表示电子转移的方向和数目.该反应中氧化剂与还原剂的物质的量之比是3:2;当氯气管道漏气时发生的现象是冒白烟
(2)碳的各类物质之间存在如下关系:C-CO2-H2CO3-CaCO3;氯的各类物质之间也存在如下相似关系:C12-C12O-HClO-NaClO.则C12O属于酸性氧化物(按性质分类),括号中物质的化学式为HClO;C12O与水反应的化学方程式为C12O+H2O=2HC1O.
(3)CuO在加热条件下与NH3反应,可表现出与((1)反应中的C12相同的性质,该性质是氧化性;CuO与NH3在加热条件下反应的化学方程式为3CuO+2NH3$\frac{\underline{\;加热\;}}{\;}$3Cu+N2↑+3H2O.
分析 (1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为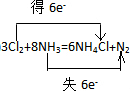 ,3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,N元素的化合价升高,生成氯化铵冒白烟,以此来解答;
,3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,N元素的化合价升高,生成氯化铵冒白烟,以此来解答;
(2)碳的各类物质之间存在如下关系:C-CO2-H2CO3-CaCO3;氯的各类物质之间也存在如下相似关系:C12-C12O-HClO-NaClO,C12O属于酸性氧化物,C12O与水反应的化学方程式为C12O+H2O=2HC1O,由此分析解答;
(3)CuO在加热条件下与NH3反应,可表现出与((1)反应中的C12相同的性质是氧化性,该性质是氧化性;反应方程式为:3CuO+2NH3$\frac{\underline{\;加热\;}}{\;}$3Cu+N2↑+3H2O.
解答 解:(1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为 ,3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,N元素的化合价升高,由反应可知3mol氧化剂与2mol还原剂反应电子守恒,则氧化剂与还原剂的物质的量之比为3:2,生成氯化铵冒白烟,故答案为:
,3Cl2+8NH3═6NH4Cl+N2中,Cl元素的化合价降低,N元素的化合价升高,由反应可知3mol氧化剂与2mol还原剂反应电子守恒,则氧化剂与还原剂的物质的量之比为3:2,生成氯化铵冒白烟,故答案为: ;3:2;冒白烟;
;3:2;冒白烟;
(2)碳的各类物质之间存在如下关系:C-CO2-H2CO3-CaCO3;氯的各类物质之间也存在如下相似关系:C12-C12O-HClO-NaClO,C12O属于酸性氧化物,C12O与水反应的化学方程式为C12O+H2O=2HC1O,故答案为:HClO;酸性氧化物;HClO;C12O+H2O=2HC1O;
(3)CuO在加热条件下与NH3反应,可表现出与((1)反应中的C12相同的性质是氧化性,该性质是氧化性;反应方程式为:3CuO+2NH3$\frac{\underline{\;加热\;}}{\;}$3Cu+N2↑+3H2O,故答案为:氧化性;3CuO+2NH3$\frac{\underline{\;加热\;}}{\;}$3Cu+N2↑+3H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

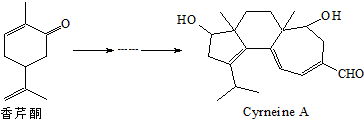
| A. | 香芹酮化学式为C9H12O | |
| B. | Cyrneine A可以发生加成反应、消去反应和氧化反应 | |
| C. | 香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色 | |
| D. | 香芹酮和Cyrneine A可以通过氯化铁溶液鉴别 |
| A. | 蒸馏时,在烧瓶中加几粒沸石 | |
| B. | 加液时,胶头滴管悬置在试管正上方 | |
| C. | 萃取时,分液漏斗正立振荡后,直接放在铁架台上,静置 | |
| D. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 二氧化氮 | D. | 一氧化氮 |
| A. | SO2为原子晶体,CO2为分子晶体 | |
| B. | 中心原子采取的杂化方式:SO2为sp2杂化,CO2为sp杂化 | |
| C. | 都是直线形结构 | |
| D. | S原子和C原子上都没有孤电子对 |
| A. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O | B. | CO2+Ca(OH)2$\frac{\underline{\;点燃\;}}{\;}$CaCO3↓+H2O | ||
| C. | Fe2O3+3CO═2Fe+3CO2 | D. | 2Na+Cl2═2NaCl |
| A. | SO2+2Fe3++2H2O═SO42-+2Fe2++4H+ | |
| B. | I2+2Fe2+═2I-+2Fe3+ | |
| C. | SO2+I2+2H2O═2I-+4H++SO42- | |
| D. | 少量Cl2通入FeI2溶液中:Cl2+2I-═2Cl-+I2 |
| A. | 氯水 | B. | 玻璃 | C. | 生铁 | D. | 液氨 |