题目内容
3.制备纳米材料TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到固体TiO2.
用氧化还原滴定法测定TiO2:
一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶
液滴定Ti3+至全部生成Ti4+(Ti3+和Ti4+在溶液中无色,与 KSCN溶液不反应),请回答下列
问题:
(1)有利于TiCl4水解生成TiO2•xH2O的条件有吸热(写出1个条件).
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是抑制NH4Fe(SO4)2水解;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的哪两种ac(填字母代号).

(3)滴定时,NH4Fe(SO4)2标准液用什么仪器盛装?酸式滴定管;滴定终点的现象是溶液变为红色,且半分钟不褪色.
(4)下列错误操作导致TiO2质量分数测定结果如何变化(填“偏高”、“偏低”或“无影响”)?
若容量瓶清洗之后,未干燥.无影响;
若在滴定终点读取滴定管刻度时,俯视标准液液面.偏低.
分析 (1)根据水解反应吸热,升高温度,水解程度增大;
(2)铁离子、铵根离子易水解,使溶液呈酸性,加酸硫酸,抑制NH4Fe(SO4)2水解;根据配制一定物质的量浓度的溶液的具体操作步骤,选择所需的仪器;
(3)根据NH4Fe(SO4)2标准液呈酸性来解答;用KSCN作指示剂,终点时NH4Fe(SO4)2不再反应,生成血红色的Fe(SCN)3;
(4)①若容量瓶清洗之后,未干燥,其物质的量不变,消耗V(标准)不变;
②若终点俯视滴定管,读取的体积比实际消耗的体积偏小,消耗V(标准)减小.
解答 解:(1)水解反应吸热,升高温度,水解程度增大,有利于TiCl4水解生成TiO2•xH2O的条件有升温;
故答案为:吸热;
(2)铁离子、铵根离子易水解,使溶液呈酸性,故需加入一定量的稀硫酸抑制抑制NH4Fe(SO4)2水解;称量NH4Fe(SO4)2需用天平、药匙,溶解需要用烧杯,量筒(也可不用),玻璃棒搅拌,转移过程中用玻璃棒引流到容量瓶中,最后用胶头滴管定容.故还需仪器为:容量瓶、胶头滴管;
故答案为:ac;
(3)NH4Fe(SO4)2标准液呈酸性,用酸式滴定管盛装;Fe3+与Ti3+反应,被还原为Fe2+,加入KSCN不显红色,当达到滴定终点时,再加入NH4Fe(SO4)2,溶液中Fe3+过量,会变成红色,且半分钟不褪色;
故答案为:酸式滴定管;溶液变为红色,且半分钟不褪色;
(4)①若容量瓶清洗之后,未干燥,其物质的量不变,消耗V(标准)不变,百分含量无影响;
故答案为:无影响;
②若终点俯视滴定管,读取的体积比实际消耗的体积偏小,消耗V(标准)减小,待测液的物质的量偏低,质量分数偏低;
故答案为:偏低.
点评 本题考查物质的制备、检验和滴定方法,题目难度中等,注意掌握化学基本实验基本操作方法,明确中和滴定操作方法及误差分析方法,试题侧重考查学生的分析、理解能力.

 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案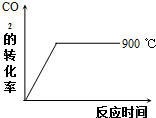 碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:
碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:(1)已知:2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1=-1214.6kJ/mol
2CO(g)+O2(g)═2CO2(g)△H2=-566kJ/mol
请写出CH4燃烧热的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
(2)在不同温度下反应CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数K如下表:
| 温度/℃ | 600 | 750 | 900 | 1100 | 1250 |
| 平衡常数K | 2.5 | 1.6 | 1 | 0.9 | 0.6 |
②900℃时发生上述反应,CO2的转化率随时间变化如图所示,若到达平衡后加压,则H2的转化率将(填“增大”、“减小”或“不变”,下同)不变,正反应速率将增大.
其他条件相同时,请在图中画出750℃时CO2的转化率随时间变化的示意图.
③在900℃时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是(填编号)AD,平衡后与C中各物质的百分含量相等的组有BD(填编号)
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 0.5 | 1 |
①放电时,负极电极反应式:CH3OCH3-12e-+16OH-=2CO32-+11H2O.
②假设该燃料电池中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为6.72L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 乙醇(乙酸) | KOH溶液 | 分液 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液.
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
| 滴定次数 | 盐酸体积 | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
(1)步骤①中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果无影响(填“偏大”、“偏小”或“无影响”).
(2)步骤②中,滴定时眼睛应注视锥形瓶(填仪器名称),判断到达滴定终点的依据是滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次的体积,其可能的原因是AB(填字母)
A.滴定前滴定管尖嘴有气泡,滴定结束时无气泡
B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成
D.滴定终点时,俯视读数
(4)根据上表记录数据,通过计算可得该盐酸的浓度为0.1626 mol•L-1.
| U | ||
| Y |
(1)元素W的原子核外共有5种不同能级的电子.
(2)下列反应在恒容密闭容器中进行:2YO2(g)+O2(g)$?_{催化剂}^{450℃}$ 2YO3(g)+190kJ
①该反应 450℃时的平衡常数大于500℃时的平衡常数(填“大于”、“小于”或“等于”).
②下列描述中能说明上述反应已达平衡的是bd
a.ν(O2)正=2ν(YO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
③在一个固定容积为5L的密闭容器中充入0.20 mol YO2和0.10molO2,半分钟后达到平衡,测得容器中含YO30.18mol,则ν(O2)=0.36mol•L-1•min-1:若继续通入0.20molYO2和0,.10molO2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36mol<n(YO3)<0.40mol.
(3)V的最简单气态氢化物甲的水溶液显碱性.
一定条件下,甲在恒容密闭容器中发生分解反应(正反应放向为吸热反应)并达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是bc.(选填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |
 已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )| A. | a点所得溶液中;2n(H2A)+n(A2-)=0.002mol | |
| B. | b点所得溶液中:c(H2A)+c(H+)=c(A2-)+e(OH-) | |
| C. | C点所得溶液中:c(Na+)<3c(HA-) | |
| D. | d点所得溶液中:c(Na+)>c(A2-)>c(HA-) |
| A. | 不粘锅的内壁有聚四氟乙烯涂层,它不能使酸性高锰酸钾溶液褪色 | |
| B. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 用于奥运“祥云”火炬的丙烷是一种清洁燃料 | |
| D. | 淀粉和纤维素的组成都是(C6H10O5)n,两者互为同分异构体,且水解最终产物都是葡萄糖 |