题目内容
4. 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )| A. | 开始时左右两室分子数相同 | B. | 反应开始后NO室压强减小 | ||
| C. | 最终容器内密度与原来相同 | D. | 最终容器内仍然有O2存在 |
分析 A、由左右两室体积相同,两容器内气体密度相同可知,两容器中气体的质量一定相等,再结合n=$\frac{m}{M}$进行判断气体的物质的量关系,据此判断;
B、发生2NO+O2=2NO2,反应后总的物质的量减少,故反应后NO室的气体物质的量要减小;
C、气体的总质量为原来一氧化氮与氧气质量之和,为NO质量的2倍,体积为左右两室的体积之和,为左室的2倍,故密度不变;
D、NO、O2的质量相等,二者物质的量之比为32:30=16:15,发生2NO+O2=2NO2,O2过量.
解答 解:A、由左右两室体积相同,两容器内气体密度相同可知,两容器中气体的质量一定相等,而NO和O2的摩尔质量不相等,故其物质的量不相等,开始时左右两室分子数不相同,故A错误;
B、发生2NO+O2=2NO2,反应后总的物质的量减少,平均充满左右两室,故反应后NO室的气体物质的量要减小,故压强减小,故B正确;
C、反应后气体的总质量为原来一氧化氮与氧气质量之和,为NO质量的2倍,体积为左右两室的体积之和,为左室的2倍,故密度不变,故C正确;
D、NO、O2的质量相等,二者物质的量之比为32:30=16:15,发生2NO+O2=2NO2,O2过量,故最终容器内有O2存在,故D正确;
故选A.
点评 本题考查阿伏伽德罗定律及推论、化学计算等,难度中等,注意二者发生反应物质的量减少,掌握基础是关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
12.取两份铝片,第一份与足量盐酸反应,第二份与足量氢氧化钠溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 1:6 |
19.下列有关说法正确的是( )
| A. | 催化剂可以加快化学反应速率,也能增大化学反应的焓变 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 25℃下,在NH3•H2O稀溶液中加水稀释,$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$的值不变 | |
| D. | 在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-电离程度减小 |
13.据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应方程如下:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g).下列叙述错误的是( )
| A. | 使用合适的催化剂可大大提高生产效率 | |
| B. | 由反应需在300℃进行,可知该反应是吸热反应 | |
| C. | 增大原料气中CO2的百分含量,可以提高H2的转化率 | |
| D. | 70MPa的压力,不仅可以增加单位时间内的产出,还可以提高CO2和H2的利用率 |

 pH(HNO3)
pH(HNO3) 2SO3(g);3Fe
2SO3(g);3Fe (s)+4H2O(g)
(s)+4H2O(g)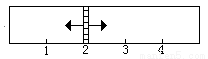
 数为______________。欲使起始反应维持向该方向进行,则x的最大值应小于____________。
数为______________。欲使起始反应维持向该方向进行,则x的最大值应小于____________。