题目内容
3.下列说法正确的是( )| A. | 在常温常压下,20mlNH3与60mlO2所含分子个数比为1:3 | |
| B. | 在化学反应中,1mol金属镁变为镁离子时失去电子数为NA | |
| C. | 在标准状况下,1mol水的体积为22.4L | |
| D. | 2molCaCl2中Cl-的数目为2NA |
分析 A.同温同压下气体摩尔体积相同,根据n=$\frac{V}{{V}_{n}}$=$\frac{N}{{N}_{A}}$可知气体分子数与体积成正比;
B.Mg为+2价金属,1molMg转化成镁离子失去2mol电子;
C.标况下水的状态不是气体;
D.2molCaCl2中含有4mol氯离子.
解答 解:A.根据n=$\frac{V}{{V}_{n}}$=$\frac{N}{{N}_{A}}$可知,相同条件下气体分子数与体积成正比,则20mlNH3与60mlO2所含分子个数比=20mL:60mL=1:3,故A正确;
B.在化学反应中,1mol金属镁变为镁离子时失去2mol电子,失去电子数为2NA,故B错误;
C.标况下水不是气体,不能使用标况下的气体摩尔体积计算,故C错误;
D.2molCaCl2中含有4mol氯离子,含有Cl-的数目为4NA,故D错误;
故选A.
点评 本题考查了物质的量的计算,题目难度中等,明确物质的量与气体摩尔体积、阿伏伽德罗常数等之间的关系即可解答,试题有利于提高学生的化学计算能力.

练习册系列答案
相关题目
10.下列物质中属于烷烃的是( )
| A. | 乙烷 | B. | 丙烯 | C. | 丙烷 | D. | 丁烷 |
11.关于2mol二氧化碳的叙述中,正确的是( )
| A. | 摩尔质量为44g | B. | 质量为88g/mol | ||
| C. | 有4mol氧原子 | D. | 分子数为6.02×1023 |
8.为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究--按如图装置(固定装置已略)进行实验:
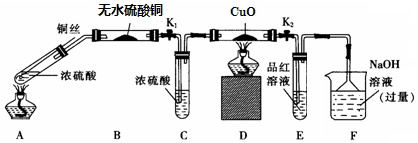
(1)F装置的烧杯中发生反应的离子方程式是SO2+2OH-=SO32-+H2O;
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是D装置中黑色固体颜色无变化,E装置中溶液褪色
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是拉起铜丝,关闭K1,K2
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是将A装置中试管内冷却后的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,若溶液变蓝,证明含有Cu2+;
,若溶液变蓝,证明含有Cu2+
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S.产生Cu2S的反应为
aCu+bH2SO4$\frac{\underline{\;\;△\;\;}}{\;}$cCu2S+dCuSO4+e H2O,则a:b=5:4
(6)为进一步探究该黑色物质的成分,经查阅相关文献获得下列资料.
资料1:
资料2:X-射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种.仅由上述资料可得出的如下结论中正确是ABD.
A.铜与浓硫酸反应时所涉及的反应可能不止一个
B.硫酸浓度选择适当,可避免最后产物中出现黑色物质
C.该反应发生的条件之一是硫酸浓度≥15mol/L
D.硫酸浓度越大,黑色物质越快出现、越难消失.
实验I:反应产物的定性探究--按如图装置(固定装置已略)进行实验:

(1)F装置的烧杯中发生反应的离子方程式是SO2+2OH-=SO32-+H2O;
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是D装置中黑色固体颜色无变化,E装置中溶液褪色
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是拉起铜丝,关闭K1,K2
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是将A装置中试管内冷却后的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,若溶液变蓝,证明含有Cu2+;
,若溶液变蓝,证明含有Cu2+
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S.产生Cu2S的反应为
aCu+bH2SO4$\frac{\underline{\;\;△\;\;}}{\;}$cCu2S+dCuSO4+e H2O,则a:b=5:4
(6)为进一步探究该黑色物质的成分,经查阅相关文献获得下列资料.
资料1:
| 硫酸/mol•L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 14 | Cu 片表面无明显现象 | |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
A.铜与浓硫酸反应时所涉及的反应可能不止一个
B.硫酸浓度选择适当,可避免最后产物中出现黑色物质
C.该反应发生的条件之一是硫酸浓度≥15mol/L
D.硫酸浓度越大,黑色物质越快出现、越难消失.
12.炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是( )
| A. | CN-可以和稀硫酸反应生成HCN | B. | CN-可被Cl2氧化成(CN)28 | ||
| C. | 在水溶液中(CN)2可被F-还原 | D. | HCN的电子式为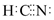 |
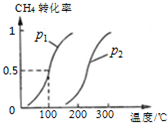 甲烷,甲醇,乙酸是化工产品的重要原料.
甲烷,甲醇,乙酸是化工产品的重要原料.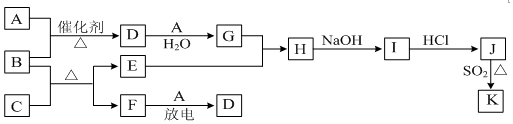
 如图是我校化学实验室浓盐酸试剂标签上的部分内容.
如图是我校化学实验室浓盐酸试剂标签上的部分内容.