题目内容
 某校化学研究性学习小组设计如下实验方案,测定放置已久的NaHCO3样品中Na2CO3的质量分数.填写下列空白.
某校化学研究性学习小组设计如下实验方案,测定放置已久的NaHCO3样品中Na2CO3的质量分数.填写下列空白.【方案一】气体吸收法:按图装置进行实验.
(碱石灰可吸收水、酸性气体)
①实验前应先
②实验中除称量样品质量外,还需称
③根据此实验得到的数据,测定结果有较大误差.因为实验装置还存在一个明显缺陷,该缺陷是
【方案二】沉淀法:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氢氧化钙溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
(1)洗涤沉淀的方法是
(2)已知称得样品9.7g,干燥后的沉淀质量为6.0g,则样品中碳酸钠的质量分数为
考点:探究物质的组成或测量物质的含量
专题:
分析:由测定含量的实验可知,A中发生Na2CO3+H2SO4=H2O+CO2↑+Na2SO4、2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,B中为浓硫酸吸收水,干燥二氧化碳,利用C装置吸收二氧化碳,D装置防止空气中的二氧化碳、水进入C装置干扰含量测定,结合反应计算含量,
方案一:①实验前应检查装置的气密性,防止装置漏气,装置B中为浓H2SO4,可干燥二氧化碳,装置D的作用为防止空气中水蒸气、CO2进入C管被吸收;
②实验中除称量样品质量外,还需要称装置C的质量变化得到二氧化碳质量进行计算;
③实验装置还存在一个明显缺陷为:装置中的二氧化碳不一定被C全部吸收,A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中,则需设计一个装置将A、B中的CO2全部吹入C中吸收,
方案二:①洗涤沉淀的方法是在过滤器中进行;
②依据沉淀质量计算碳酸钠质量得到质量分数;
方案一:①实验前应检查装置的气密性,防止装置漏气,装置B中为浓H2SO4,可干燥二氧化碳,装置D的作用为防止空气中水蒸气、CO2进入C管被吸收;
②实验中除称量样品质量外,还需要称装置C的质量变化得到二氧化碳质量进行计算;
③实验装置还存在一个明显缺陷为:装置中的二氧化碳不一定被C全部吸收,A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中,则需设计一个装置将A、B中的CO2全部吹入C中吸收,
方案二:①洗涤沉淀的方法是在过滤器中进行;
②依据沉淀质量计算碳酸钠质量得到质量分数;
解答:
解:由测定含量的实验可知,A中发生Na2CO3+H2SO4=H2O+CO2↑+Na2SO4、2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,B中为浓硫酸吸收水,干燥二氧化碳,利用C装置吸收二氧化碳,D装置防止空气中的二氧化碳、水进入C装置干扰含量测定,
方案一:①实验前应检查装置的气密性,防止装置漏气,装置B中为浓H2SO4,可干燥二氧化碳,装置D的作用为防止空气中水蒸气、CO2进入C管被吸收,
故答案为:检查装置的气密性;防止空气中水蒸气、CO2进入C装置被吸收;
②实验中除称量样品质量外,还需要称这种C的质量变化得到二氧化碳质量进行计算,
故答案为:C;
③实验装置还存在一个明显缺陷为:装置中的二氧化碳不一定被C全部吸收,A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中,则需设计一个装置将A、B中的CO2全部吹入C中吸收,
故答案为:A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中;
方案二:①洗涤沉淀的方法是在过滤器中进行,向过滤器中加入蒸馏水至液面没过沉淀,待水自然流净后重复操作两到三次,
故答案为:向过滤器中加入蒸馏水至液面没过沉淀,待水自然流净后重复操作两到三次;
②样品5.7g,干燥后的沉淀质量为6.0g为CaCO3的质量,则样品中碳酸钠的质量分数:
×100%=65.6%,
故答案为:65.6.
方案一:①实验前应检查装置的气密性,防止装置漏气,装置B中为浓H2SO4,可干燥二氧化碳,装置D的作用为防止空气中水蒸气、CO2进入C管被吸收,
故答案为:检查装置的气密性;防止空气中水蒸气、CO2进入C装置被吸收;
②实验中除称量样品质量外,还需要称这种C的质量变化得到二氧化碳质量进行计算,
故答案为:C;
③实验装置还存在一个明显缺陷为:装置中的二氧化碳不一定被C全部吸收,A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中,则需设计一个装置将A、B中的CO2全部吹入C中吸收,
故答案为:A装置中产生的CO2未全部被C装置吸收,有部分滞留在A装置中;
方案二:①洗涤沉淀的方法是在过滤器中进行,向过滤器中加入蒸馏水至液面没过沉淀,待水自然流净后重复操作两到三次,
故答案为:向过滤器中加入蒸馏水至液面没过沉淀,待水自然流净后重复操作两到三次;
②样品5.7g,干燥后的沉淀质量为6.0g为CaCO3的质量,则样品中碳酸钠的质量分数:
| ||
| 9.7g |
故答案为:65.6.
点评:本题考查碳酸氢钠含量的测定实验,为高频考点,题目难度中等,把握实验装置的作用及实验目的为解答的关键,侧重分析、计算及实验能力的综合考查.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列表示物质结构的化学用语正确的是( )
| A、乙烯的结构简式CH2CH2 |
| B、Na2O2中氧元素的化合价为-2 |
C、Cl-的结构示意图: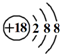 |
| D、乙烷的结构简式:CH3CH3 |
下列性质的递变中,正确的是( )
| A、O、S、Na的原子半径依次减小 |
| B、LiOH、KOH、CsOH的碱性依次增强 |
| C、HF、NH3、SiH4的稳定性依次增强 |
| D、HCl、HBr、HI的还原性依次减弱 |
下列说法正确的是( )
| A、共价化合物中可能含有离子键 |
| B、最外层有2个电子的原子一定在ⅡA族 |
| C、离子化合物中可能含共价键 |
| D、H2O的稳定性很强是因为其分子间能形成氢键 |
下列反应中,不属于氧化还原反应却是吸热反应的是( )
| A、Ca(OH)2和NH4Cl反应 |
| B、钢铁生锈 |
| C、H2与CuO高温反应 |
| D、乙醇与O2的燃烧反应 |
能正确表示下列反应的离子方程式是( )
| A、将Cl2通入溴化亚铁溶液:2Br-+Cl2═Br2+2Cl- |
| B、用稀硫酸吸收氨气:NH3+H+═NH4+ |
| C、AlCl3溶液中加入过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4+ |
| D、碳酸氢钠和稀硫酸反应:CO32-+2H+═CO2↑+H2O |
 用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如表所示,
用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如表所示,
