题目内容
现有A、B、C、D、E、F六种化合物,它们分别由下列五种原子团中的两种不同基团组成:-CH3、-OH、-C6H5、-COOH、-CHO
①A是无色晶体,有特殊气味,在空气中会逐渐变成粉红色;
②B、C、F都能发生银镜反应,B.C均能加氢变成醇,C的相对分子质量大于B,F的相对分子质量小于D;
③D的水溶液可以和少量氢氧化钠溶液反应生成一种化合物,生成-1价的阴离子,也可和过量的氢氧化钠反应,生成-2价阴离子.D可以和A的钠盐反应生成A;
④E是由B氧化而成.
试回答下列问题:
(1)写出A、D、F的结构简式:A D F
(2)B发生银镜反应的化学方程式
(3)C与足量氢气反应的化学方程式
(4)上述具有酸性的化合物中,酸性由强到弱的顺序为 (填结构简式)
①A是无色晶体,有特殊气味,在空气中会逐渐变成粉红色;
②B、C、F都能发生银镜反应,B.C均能加氢变成醇,C的相对分子质量大于B,F的相对分子质量小于D;
③D的水溶液可以和少量氢氧化钠溶液反应生成一种化合物,生成-1价的阴离子,也可和过量的氢氧化钠反应,生成-2价阴离子.D可以和A的钠盐反应生成A;
④E是由B氧化而成.
试回答下列问题:
(1)写出A、D、F的结构简式:A
(2)B发生银镜反应的化学方程式
(3)C与足量氢气反应的化学方程式
(4)上述具有酸性的化合物中,酸性由强到弱的顺序为
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A、B、C、D、E、F六种化合物,它们分别由下列五种原子团中的两种不同基团组成:-CH3、-OH、-C6H5、-COOH、-CHO,①A是无色晶体,有特殊气味,在空气中会逐渐变成粉红色,所以A为HO-C6H5;②B、C、F都能发生银镜反应,说明它们都有醛基,B.C均能加氢变成醇,C的相对分子质量大于B,所以C为C6H5-CHO,B为CH3-CHO;③D的水溶液可以和少量氢氧化钠溶液反应生成一种化合物,生成-1价的阴离子,也可和过量的氢氧化钠反应,生成-2价阴离子,D可以和A的钠盐反应生成A,所以D为HO-COOH,F的相对分子质量小于D且有醛基,所以F为HO-CHO;④E是由B氧化而成,所以E为CH3-COOH,据此答题.
解答:
解:A、B、C、D、E、F六种化合物,它们分别由下列五种原子团中的两种不同基团组成:-CH3、-OH、-C6H5、-COOH、-CHO,①A是无色晶体,有特殊气味,在空气中会逐渐变成粉红色,所以A为HO-C6H5;②B、C、F都能发生银镜反应,说明它们都有醛基,B.C均能加氢变成醇,C的相对分子质量大于B,所以C为C6H5-CHO,B为CH3-CHO;③D的水溶液可以和少量氢氧化钠溶液反应生成一种化合物,生成-1价的阴离子,也可和过量的氢氧化钠反应,生成-2价阴离子,D可以和A的钠盐反应生成A,所以D为HO-COOH即为H2CO3,F的相对分子质量小于D且有醛基,所以F为HO-CHO;④E是由B氧化而成,所以E为CH3-COOH,
(1)根据上面的分析可知,A为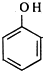 ,D为HO-COOH,F为HCOOH,故答案为;
,D为HO-COOH,F为HCOOH,故答案为; ;HO-COOH;HCOOH;
;HO-COOH;HCOOH;
(2)B为CH3CHO,发生银镜反应的化学方程式为CH3CHO+2Ag(NH3)OH
CH3COONH4+2Ag↓+3NH3+H2O,
故答案为:CH3CHO+2Ag(NH3)OH
CH3COONH4+2Ag↓+3NH3+H2O;
(3)C为C6H5-CHO,与足量氢气发生加成反应,反应的化学方程式为C6H5-CHO+4H2
 ,故答案为:C6H5-CHO+4H2
,故答案为:C6H5-CHO+4H2
 ;
;
(4)上述具有酸性的化合物有 、H2CO3、CH3COOH、HCOOH,它们酸性由强到弱的顺序为HCOOH>CH3COOH>H2CO3>
、H2CO3、CH3COOH、HCOOH,它们酸性由强到弱的顺序为HCOOH>CH3COOH>H2CO3> ,
,
故答案为:HCOOH>CH3COOH>H2CO3> .
.
(1)根据上面的分析可知,A为
 ,D为HO-COOH,F为HCOOH,故答案为;
,D为HO-COOH,F为HCOOH,故答案为; ;HO-COOH;HCOOH;
;HO-COOH;HCOOH; (2)B为CH3CHO,发生银镜反应的化学方程式为CH3CHO+2Ag(NH3)OH
| △ |
故答案为:CH3CHO+2Ag(NH3)OH
| △ |
(3)C为C6H5-CHO,与足量氢气发生加成反应,反应的化学方程式为C6H5-CHO+4H2
| 催化剂 |
 ,故答案为:C6H5-CHO+4H2
,故答案为:C6H5-CHO+4H2| 催化剂 |
 ;
; (4)上述具有酸性的化合物有
 、H2CO3、CH3COOH、HCOOH,它们酸性由强到弱的顺序为HCOOH>CH3COOH>H2CO3>
、H2CO3、CH3COOH、HCOOH,它们酸性由强到弱的顺序为HCOOH>CH3COOH>H2CO3> ,
,故答案为:HCOOH>CH3COOH>H2CO3>
 .
.
点评:本题主要考查了根据性质确定官能团,难度不大,答题时要熟记常见有机官能 团的性质及常见有机反应方程式的书写.

练习册系列答案
相关题目
下列实验方法正确的是( )
| A、从溴水中提取溴可用酒精作为萃取剂 |
| B、检验碘化钾溶液可用淀粉 |
| C、分离碘和食盐可用加热的方法 |
| D、用加热的方法除去铜中混有的氧化铜 |
将16gFeS与FeO的混合物,投入到1L1mol/L的硝酸溶液中充分反应,只产生
molNO气体,得到澄清的混合溶液.下列计算结果正确的是 ( )
| 1 |
| 3 |
| A、混合物中含有0.5molFeS |
| B、混合物中含有0.1mol FeO |
| C、参加反应的HNO3为1mol |
| D、氧化产物Fe3+为0.15mol |
某芳香烃A(分子式为C9H10,含有一个碳碳双键)有如下转化关系: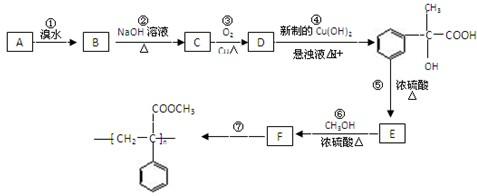
按要求填空:
(1)写出反应①的反应类型 ;反应⑤的反应类型 ;
(2)写出A和F结构简式:A ;F ;
(3)写出反应③的化学方程式: .

按要求填空:
(1)写出反应①的反应类型
(2)写出A和F结构简式:A
(3)写出反应③的化学方程式:
下列说法正确的是( )
| A、煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 |
| B、石油分馏得到的汽油、煤油、柴油等都有固定的熔沸点 |
| C、石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等) |
| D、电解冶炼铝的原料是氯化铝 |
下表是3种物质的溶解度(20℃),下列说法中正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g) | 74 | 0.0009 | 0.02 |
| A、已知MgCO3的Ksp=6.8×10-6(mol?L-1)2,则所有含固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.8×10-6 (mol?L-1)2 |
| B、将MgCl2与水混合,再对溶液蒸干、灼烧,最终所得固体产物为MgO |
| C、除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液 |
| D、用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+MgCO3↓+2H2O |
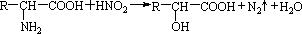
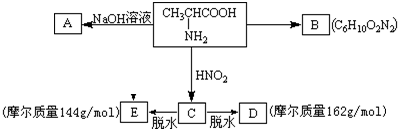
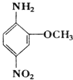 织物的染色,也用于制一些有机颜料,若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)为( )
织物的染色,也用于制一些有机颜料,若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)为( )