题目内容
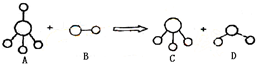
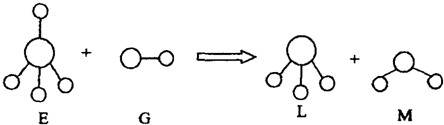
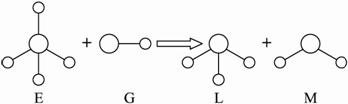
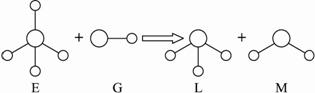
已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(组成A、B、C、D微粒的元素原子序数均小于10)。回答下列问题:
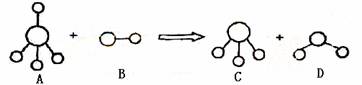
①在A、B、C、D所含的原子中未成对电子数最多的原子的电子排布式为 。
②C分子是 (“极性”或“非极性)分子,D分子的晶体的熔沸点明显高于同主族的组成相似的分子晶体的熔沸点的原因是 。
①1s22s22p3 ②极性,水分子间存在氢键

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目