题目内容
(1)有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融硝酸钾;⑥乙醇; ⑦稀硫酸; ⑧金刚石; ⑨二氧化硫; ⑩冰醋酸.
属于非电解质的有 ;属于强电解质的有 ;(填序号)
(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈 性,溶液中c(NH4+)与c(Cl-)的大小关系是:c(NH4+) c(Cl-);
(3)常温下,0.010mol?L-1盐酸和0.010mol?L-1氨水的pH之和 14,常温下,pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和 14(填>,<或=)
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水溶液20mL,消耗盐酸12.5mL,则此氨水物质的量浓度为 mol?L-1.
属于非电解质的有
(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈
(3)常温下,0.010mol?L-1盐酸和0.010mol?L-1氨水的pH之和
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水溶液20mL,消耗盐酸12.5mL,则此氨水物质的量浓度为
考点:酸碱混合时的定性判断及有关ph的计算,电解质与非电解质,强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:(1)电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物,非金属氧化物、大多数的有机物(如蔗糖、乙醇等),单质,混合物既不是电解质也不是非电解质;强电解在水溶液中完全电离的电解质;
(2)氨水为弱碱,溶液中部分电离,二者等体积混合后氨水过量,溶液显示碱性;根据电荷守恒判断溶液中c(NH4+)与c(Cl-)的大小;
(3)常温下,0.010mol?L-1盐酸的PH=2和0.010mol?L-1氨水的pH小于12,两者PH之和小于14;常温下,pH=2的盐酸加水稀释10倍后,和pH=3,而pH=12的氨水,加水稀释10倍后,溶液的PH减小不到1单位,两溶液的pH之和大于14;
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水,达到终点时消耗盐酸溶液12.5mL,利用c酸V酸=c碱V碱计算;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物,非金属氧化物、大多数的有机物(如蔗糖、乙醇等),单质,混合物既不是电解质也不是非电解质;强电解在水溶液中完全电离的电解质;
(2)氨水为弱碱,溶液中部分电离,二者等体积混合后氨水过量,溶液显示碱性;根据电荷守恒判断溶液中c(NH4+)与c(Cl-)的大小;
(3)常温下,0.010mol?L-1盐酸的PH=2和0.010mol?L-1氨水的pH小于12,两者PH之和小于14;常温下,pH=2的盐酸加水稀释10倍后,和pH=3,而pH=12的氨水,加水稀释10倍后,溶液的PH减小不到1单位,两溶液的pH之和大于14;
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水,达到终点时消耗盐酸溶液12.5mL,利用c酸V酸=c碱V碱计算;
解答:
解:(1)电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物,非金属氧化物、大多数的有机物(如蔗糖、乙醇等),单质,混合物既不是电解质也不是非电解质;强电解在水溶液中完全电离的电解质,所以非电解质的有⑥⑨属于强电解质的有②④⑤,故答案为:⑥⑨、②④⑤;
(2)将pH=3的盐酸和pH=11的氨水等体积混合,氨水部分电离,混合后氨水过量,溶液显示碱性,则c(H+)<c(OH-);根据电荷守恒可知:c(NH4+)+c(H+)=c(OH-)+c(Cl-),所以溶液中c(NH4+)>c(Cl-),
故答案为:碱;>;
(3)常温下,0.010mol?L-1盐酸的PH=2和0.010mol?L-1氨水的pH小于12,两者PH之和小于14;常温下,pH=2的盐酸加水稀释10倍后,和pH=3,而pH=12的氨水,加水稀释10倍后,溶液的PH减小不到1单位,两溶液的pH之和大于14,故答案为:<;>;
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水溶液20mL,达到终点时消耗盐酸溶液12.5mL,由c酸V酸=c碱V碱可知,12.5×10-3L×0.04mol/L=c碱×20×10-3L,
解得c碱=0.025mol/L,所以氨水物质的量浓度为0.025mol/L;故答案为:0.025.
非电解质是指:在水溶液里和熔融状态下都不导电的化合物,非金属氧化物、大多数的有机物(如蔗糖、乙醇等),单质,混合物既不是电解质也不是非电解质;强电解在水溶液中完全电离的电解质,所以非电解质的有⑥⑨属于强电解质的有②④⑤,故答案为:⑥⑨、②④⑤;
(2)将pH=3的盐酸和pH=11的氨水等体积混合,氨水部分电离,混合后氨水过量,溶液显示碱性,则c(H+)<c(OH-);根据电荷守恒可知:c(NH4+)+c(H+)=c(OH-)+c(Cl-),所以溶液中c(NH4+)>c(Cl-),
故答案为:碱;>;
(3)常温下,0.010mol?L-1盐酸的PH=2和0.010mol?L-1氨水的pH小于12,两者PH之和小于14;常温下,pH=2的盐酸加水稀释10倍后,和pH=3,而pH=12的氨水,加水稀释10倍后,溶液的PH减小不到1单位,两溶液的pH之和大于14,故答案为:<;>;
(4)用物质的量浓度为0.04mol?L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol?L-1的氨水溶液20mL,达到终点时消耗盐酸溶液12.5mL,由c酸V酸=c碱V碱可知,12.5×10-3L×0.04mol/L=c碱×20×10-3L,
解得c碱=0.025mol/L,所以氨水物质的量浓度为0.025mol/L;故答案为:0.025.
点评:本题考查电解质、非电解质概念的辨析以及注意掌握酸碱混合的计算公式、离子反应的书写,根据酸碱的性质确定混合溶液酸碱性,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| B、温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变 |
| C、8NH3(g)+6NO2(g)═7N2(g)+12H2O(g)△H<0,则该反应一定能自发进行 |
| D、由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 |
一定量的某有机物完全燃烧后,生成1mol CO2和9g H2O,该有机物可能是( )
| A、C2H4 |
| B、CH3CH2OH |
| C、CH3CHO |
| D、C2H2 |
下列判断中正确的是( )
| A、在标准状况下,1mol水的体积约为22.4L |
| B、标准状况下,氧气的气体摩尔体积约为22.4L?mol-1 |
| C、常温常压下,1mol氢气的体积为22.4L |
| D、常温常压下,1mol氧气的质量为32克 |
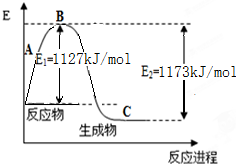 氨气是一种重要的化工原料,工业上用N2和H2合成NH3.现已知N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图如图.回答下列问题:
氨气是一种重要的化工原料,工业上用N2和H2合成NH3.现已知N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图如图.回答下列问题:
 如图1所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的N2和H2使三容器压强相等,一定条件下发生N2+3H2?2NH3的反应.问:
如图1所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的N2和H2使三容器压强相等,一定条件下发生N2+3H2?2NH3的反应.问: