题目内容
17.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 16 gO2中含有的氧分子数为NA | |
| B. | 1 mol镁原子中含有的电子数为NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1L 1 mol/L BaCl2溶液中含有的钡离子数为NA |
分析 A、氧气分子个数N=$\frac{m}{M}{N}_{A}$;
B、镁原子中含12个电子;
C、常温常压下气体摩尔体积大于22.4L/mol;
D、求出氯化钡的物质的量,然后根据1mol氯化钡中含1mol钡离子来分析.
解答 解:A、氧气分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{16g}{32g/mol}{N}_{A}$=0.5NA个,故A错误;
B、镁原子中含12个电子,故1mol镁原子中含12NA个电子,故B错误;
C、常温常压下气体摩尔体积大于22.4L/mol,故11.2L氢气的物质的量小于0.5mol,则含有的氢气分子个数小于0.5NA个,故C错误;
D、溶液中氯化钡的物质的量n=CV=1mol/L×1L=1mol,而1mol氯化钡中含1mol钡离子,故1mol氯化钡中含NA个钡离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
8.下列数据有些明显不符合事实.其中不可信的是( )
| A. | H-Cl的键能为432 kJ/mol,H-F的键能明显高于432 kJ/mol | |
| B. | 0.1 mol/L氨水中NH3•H2O部分电离,一定温度下该氨水的电离度为55% | |
| C. | 某Ca(OH)2溶液的浓度为0.5 mol/L | |
| D. | 十六烷的裂化产物中不饱和烃的分子数超过50% |
12.香兰素是重要的香料之一,它可由丁香酚合成,如图所示,有关两种化合物的说法正确的是( )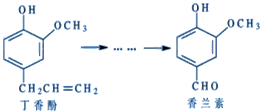

| A. | 常温下,1 mol丁香酚只能与1 mol Br2反应 | |
| B. | 丁香酚不能与FeCl3溶液发生显色反应 | |
| C. | 1 mol香兰素最多能与3 mol氢气发生加成反应 | |
| D. | 香兰素分子中至少有12个原子共平面 |
2.下列反应属于吸热反应的是( )
| A. | 2Na+O2$\frac{\underline{\;点燃\;}}{\;}$ Na2O2 | B. | HCl+NaOH═NaCl+H2O | ||
| C. | 2CaSO4═2CaO+2SO2↑+O2↑ | D. | Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 |
9.给出化学式的下列物质中,其俗名和所属分类都正确的是( )
| A. | NaOH:苛性钠 电解质 | B. | CHCl3:氯仿 盐 | ||
| C. | CH3COOH:醋酸 离子化合物 | D. | CuSO4•5H2O:胆矾 混合物 |
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 遇到石蕊试液变红的溶液:Na+、NH4+、K+、NO3- | |
| B. | 遇[Fe(CN)6]3-产生蓝色沉淀的溶液:Ca 2+、Cl-、ClO-、Fe3+ | |
| C. | 水电离出的c(OH-)=1×10-12 mol/L的溶液:S2O3-、Cl-、NO3-、Na+ | |
| D. | 与铝反应产生大量氢气的溶液:Ba 2+、HCO3-、I-、Fe3+ |
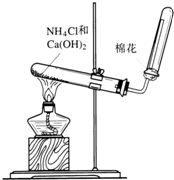 如图是实验室制取氨气的装置图.请回答:
如图是实验室制取氨气的装置图.请回答: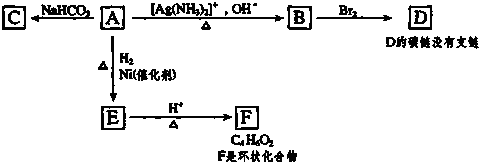
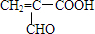 ;
;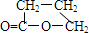 ,由E生成F的反应类型是酯化反应.
,由E生成F的反应类型是酯化反应.