题目内容
17.已知有机化合物X中各元素的质量分数分别为C---60%,H---13.3%,O---26.7%.请填空:
(1)有机物X的实验式为C3H8O.若0.1molX在足量氧气中充分燃烧需消耗氧气10.08L(标准状况),则X的分子式为C3H8O.
(2)实验表明:X能与金属钠反应产生H2.X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3:2:2:1,则X分子中含有的官能团的名称为羟基,X的结构简式为CH3CH2CH2OH.
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2,而Z不能.则Y、Z的结构简式分别为CH3CHOHCH3、CH3OCH2CH3.
分析 (1)根据相对原子质量及元素的质量分数来计算某化合物X中原子的个数之比,即实验式;
(2)根据实验式中碳原子已饱和,则分子式也就是实验式,然后根据X能与金属钠反应产生H2,说明含有羟基,不同氢原子在核磁共振氢谱中对应不同的峰,且峰的面积与氢原子数成正比求出结构简式;
(3)CH3CH2CH2OH的同分异构体有2-丙醇和甲乙醚,2-丙醇与金属钠反应产生H2,甲乙醚金属钠反应产生H2.
解答 解:(1)分子中碳、氢、氧原子的个数之比为:$\frac{60%}{12}$:$\frac{13.3%}{1}$:$\frac{26.7%}{16}$=3:8:1,所以该有机物的实验式为C3H8O;
设X的化学式为(C3H8O)x,0.1molX在空气中充分燃烧需消耗标况下氧气10.08L,则0.1x×(3+$\frac{8}{4}$-$\frac{1}{2}$)×22.4=10.08,解得:x=1,则X分子式为C3H8O,
故答案为:C3H8O;C3H8O;
(2)实验式中碳原子已饱和,所以分子式也为C3H8O,X能与金属钠反应产生H2,说明含有羟基,分子的核磁共振氢谱中有4个吸收峰,且面积之比为3:2:2:1,即有4种氢原子,个数之比为3:2:2:1,结构简式为CH3CH2CH2OH;
故答案为:羟基、CH3CH2CH2OH;
(3)CH3CH2CH2OH的同分异构体有2-丙醇和甲乙醚,2-丙醇与金属钠反应产生H2,甲乙醚金属钠反应产生H2,2-丙醇的结构简式为CH3CHOHCH3,甲乙醚的结构简式为CH3OCH2CH3,
故答案为:CH3CHOHCH3;CH3OCH2CH3.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,明确常见有机物组成、结构与性质为解答关键,注意掌握守恒思想在确定有机物分子式的方法,试题培养了学生的分析能力及化学计算能力.

 名校课堂系列答案
名校课堂系列答案| A. | 四种元素位于同一周期 | B. | 氢化物的稳定性:H2Y>HZ | ||
| C. | 原子序数a>b>d>c | D. | a+3=c-2 |
| A. | 某ⅡA族元素的原子序数为a,则原子序数为a+1的元素一定是ⅢA族元素 | |
| B. | 除短周期外,其他周期均有32种元素 | |
| C. | 原子最外层只有2个电子的元素可能是金属元素也可能是非金属元素 | |
| D. | 碱金属元素是指ⅠA族的所有元素 |
| A. | Li在氧气中燃烧主要生成Li2O2 | |
| B. | At位于第七周期第ⅦA族,其气态氢化物的稳定性比HCl的强 | |
| C. | 卤族元素单质的熔、沸点随原子序数的增大而升高 | |
| D. | 第二周期非金属元素的气态氢化物溶于水后所得水溶液均呈酸性 |
| A. | K+、Na+、HCO3-、Cl- | B. | K+、MnO4-、Br-、Cl- | ||
| C. | Na+、Cl-、NO3-、SO42- | D. | Al3+、NH4+、Cl-、SO42- |
| A. | 硅酸:粘合剂、耐火材料 | B. | 硅胶:干燥剂、吸附剂、催化剂载体 | ||
| C. | 碳化硅:砂纸、砂轮 | D. | 分子筛:吸附剂、催化剂 |
| A. | 产生苍白色火焰 | B. | 产生淡黄色火焰 | C. | 出现火星四射 | D. | 产生耀眼白光 |
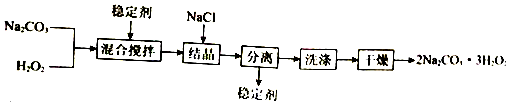
下列说法不正确的是( )
| A. | 可以用MnO2作稳定剂 | |
| B. | “结晶”时,加入NaCl的主要作用是增大产品的产率 | |
| C. | “分离”所用的主要玻璃仪器为烧杯、漏斗、玻璃棒 | |
| D. | 2Na2CO3•3H2O2受热分解属于氧化还原反应 |
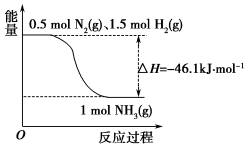 氨在工农业生产中应用广泛.
氨在工农业生产中应用广泛.