题目内容
在标准状况下:①8.96L CO2②14g CO③0.3mol SO2④3.612×1023个H2O,物质体积最大的是( )
| A、④ | B、② | C、③ | D、① |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算CO的物质的量,根据V=nVm计算CO、SO2体积,根据n=
计算水的物质的量,根据m=nM计算水的质量,再根据V=
计算水的体积,据此判断.
| m |
| M |
| N |
| NA |
| m |
| ρ |
解答:
解:①8.96L CO2;
②14g CO的物质的量=
=0.5mol,标况下其体积=0.5mol×22.4L/mol=11.2L;
③标况下0.3mol SO2的体积=0.3mol×22.4L/mol=6.72L,
④3.612×1023个H2O的物质的量=
=0.6mol,其质量=0.6mol×18g/mol=10.8g,密度约是1g/mol,故其体积约是
=10.8mL,
故14gCO的体积最大,
故选B.
②14g CO的物质的量=
| 14g |
| 18g/mol |
③标况下0.3mol SO2的体积=0.3mol×22.4L/mol=6.72L,
④3.612×1023个H2O的物质的量=
| 3.612×1023 |
| 6.02×1023mol-1 |
| 10.8g |
| 1g/mL |
故14gCO的体积最大,
故选B.
点评:本题考查物质的量的有关计算,比较基础,注意对公式的理解与灵活运用.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
常温下,0.1mol/L的氯化铵水溶液中,下列描述及关系正确的是( )
| A、溶液呈碱性 |
| B、c(NH3?H2O)+c(NH4+)=0.1mol/L |
| C、c(NH4+)+c(H+)=c(OH-)+c(Cl-) |
| D、氯化铵的加入可促进水的电离,使Kw>1.0×10-14 |
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A、X、Y、Z中最简单氢化物稳定性最弱的是Z |
| B、Z和Y元素的氧化物对应水化物的酸性Z一定强于Y |
| C、简单阴离子的还原性:X<Y |
| D、最简单氢化物的沸点:X<Y |
相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A、C3H4和C2H6 |
| B、C3H6和C3H8O |
| C、C3H6O2和C3H8O |
| D、C3H8O和C4H8O2 |
对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列各项对示意图的解释与图象相符的是( )
A、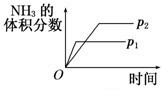 压强对反应的影响(p2>p1) |
B、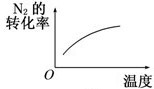 温度对反应的影响 |
C、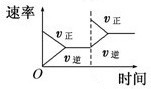 平衡体系增加N2对反应的影响 |
D、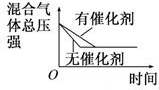 催化剂对反应的影响 |
 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )| A、原子半径的大小顺序为:rZ>rW>rX>rY |
| B、元素W的含氧酸的酸性一定比Z的含氧酸的酸性强 |
| C、工业上是通过电解法获得元素W的单质 |
| D、XZ2和XW4中化学键的类型不同 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、2.4g金属镁变为镁离子时失去的电子数为0.2NA |
| B、2.7g金属铝所含电子数目为0.3NA |
| C、0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |
| D、在常温常压下,11.2L Cl2含有的分子数为0.5NA |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、5.6g铁片投入到冷的浓硫酸中,铁片失去电子数为0.3NA |
| B、16g CH4中含有4NA个C-H键 |
| C、标准状况下,3g NO与1.6g O2混合气体所含有的分子数为0.1NA |
| D、标准状况下,5.6L四氯化碳含有的分子数为0.25NA |