题目内容
15.下列各物质所含原子数按由大到小的顺序排列为③①④②(填序号).①0.5 mol CO2;②标准状况下,22.4L氦气; ③4℃时,18mL 水;④0.2mol H2SO4.
分析 分别根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算出各物质含有原子的物质的量,然后根据根据N=nNA计算出各选项中含有原子的数目,注意稀有气体为单原子分子.
解答 解:①0.5 mol CO2含有的原子数为:0.5×3NA=1.5NA;
②氦气为单原子分子,标准状况下22.4L氦气的原子数为:$\frac{22.4L}{22.4L/mol}$=NA;
③4℃时18mL水的质量为18g,原子数为:$\frac{18g}{18g/mol}$×3NA=3NA;
④0.2mol H2SO4的原子数为:0.2×7NA=1.4NA,
各物质所含原子数按由大到小的顺序排列为:③①④②,
故答案为:③①④②.
点评 本题考查物质的量的相关计算,题目难度不大,侧重于分析、计算能力的考查,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的关系.

练习册系列答案
相关题目
6.丙酮和碘在酸性溶液中发生下列反应:CH3COCH3(aq)+I2(aq)→CH3COCH2I(l)+HI(aq).下列条件的改变对该反应的反应速率几乎无影响的是( )
| A. | 增大c(CH3COCH3) | B. | 增大c(I2) | C. | 升高温度 | D. | 增大压强 |
3.在C(s)+CO2(g)?2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强 ②增加碳的量 ③通入CO2④恒容下充入He ⑤恒压下充入He ⑥加热其中能够使反应速率增大的措施是( )
| A. | ①④ | B. | ②③⑤ | C. | ①③⑥ | D. | ①②④ |
7.由Na、Mg、Al、Zn四种金属中的两种组成的混合物30g,与足量的稀硫酸反应生成1g氢气,则混合物中必定有的金属是( )
| A. | Na | B. | Mg | C. | Al | D. | Zn |
 化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数.
化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数.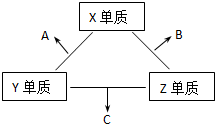 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: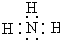 ,C分子的结构呈三角锥形.
,C分子的结构呈三角锥形. ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为: +(CH3CO)2O$→_{85-90℃}^{浓硫酸}$
+(CH3CO)2O$→_{85-90℃}^{浓硫酸}$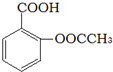 +CH3COOH操作流程如下:
+CH3COOH操作流程如下:
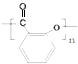 .
. .
.