题目内容
在由Cu片、Zn片和200mL稀H2SO4组成的原电池中,当Cu片上放出2.24L(标准状况下)H2时,H2SO4恰好用完.试计算:
(1)该过程中通过导线的电子的物质的量;
(2)锌片溶解的质量;
(3)原稀H2SO4的物质的量浓度.
(1)该过程中通过导线的电子的物质的量;
(2)锌片溶解的质量;
(3)原稀H2SO4的物质的量浓度.
考点:原电池和电解池的工作原理
专题:
分析:(1)根据氢气与转移电子的关系计算;
(2)根据氢气与锌的关系式计算;
(3)先根据氢气与硫酸的关系式计算硫酸的物质的量,再根据物质的量浓度公式计算.
(2)根据氢气与锌的关系式计算;
(3)先根据氢气与硫酸的关系式计算硫酸的物质的量,再根据物质的量浓度公式计算.
解答:
解:(1)设转移电子xmol,
该反应的方程式为Zn+H2SO4=ZnSO4+H2↑ 转移电子
22.4L 2mol
2.24L xmol
x=0.2
答:该过程中通过导线的电子的物质的量为0.2mol;
(2)设消耗锌yg,
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
yg 2.24L
y=6.5
答:锌片溶解的质量6.5g;
(3)设硫酸的物质的量为zmol.
Zn+H2SO4=ZnSO4+H2↑
1mol 22.4L
zmol 2.24L
z=0.1mol
C=
=0.5 mol/L
答:原稀H2SO4的物质的量浓度为0.5mol/L.
该反应的方程式为Zn+H2SO4=ZnSO4+H2↑ 转移电子
22.4L 2mol
2.24L xmol
x=0.2
答:该过程中通过导线的电子的物质的量为0.2mol;
(2)设消耗锌yg,
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
yg 2.24L
y=6.5
答:锌片溶解的质量6.5g;
(3)设硫酸的物质的量为zmol.
Zn+H2SO4=ZnSO4+H2↑
1mol 22.4L
zmol 2.24L
z=0.1mol
C=
| n |
| V |
答:原稀H2SO4的物质的量浓度为0.5mol/L.
点评:本题以原电池为载体考查了氧化还原反应的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意结合反应的方程式计算,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 30mL盐酸 | 30mL盐酸 | 30mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、向50 mL盐酸中加入混合物27.6 g时,盐酸过量 |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、15.7 g混合物与盐酸恰好能完全反应 |
| D、盐酸的物质的量浓度为5.0 mol/L |
下物质间的转化通过一步化学反应不能实现的是( )
| A、Na→NaOH |
| B、Al2O3→Al(OH)3 |
| C、Fe→FeCl2 |
| D、Fe(OH)2→Fe(OH)3 |
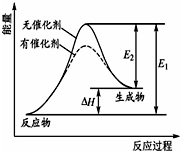 某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变反应的焓变 |
| C、催化剂能降低反应的活化能E1和 E2 |
| D、增大反应物的浓度,可使单位体积内活化分子百分数增大,反应速率加快 |
下列事实不能用勒夏特列原理解释的是( )
| A、Fe(SCN)3溶液中存在Fe3++3SCN- Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深 |
| B、用通过盛饱和食盐水的洗气瓶来除去氯气中的少量HCl气体杂质 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
| D、合成氨:N2(g)+3H2(g)?2NH3 (g)△H<0在高温、高压和催化剂条件下进行 |
25℃时,10mL 0.1mol.L-1NH4Cl溶液中存在平衡:NH4++H2O?NH3?H2O+H+.对于该平衡,下列叙述正确的是( )
| A、加入大量水稀释时,平衡向右移动,溶液中c(H+)减小 |
| B、加入几滴浓盐酸,平衡向左移动,溶液的pH值增大 |
| C、加入几滴浓氨水,平衡向逆反应方向移动,c(OH-)减小 |
| D、升温至35℃,平衡向右移动,NH4Cl的水解程度减小 |
下列溶液中氯离子浓度最小的是( )
| A、200 mL 1 mol?L-1NaCl溶液 |
| B、50 mL 0.5 mol?L-1AlCl3溶液 |
| C、100 mL 0.8 mol?L-1MgCl2溶液 |
| D、200 mL 2 mol?L-1KCl溶液 |
下列离子方程式书写正确的是( )
| A、铜与稀硝酸的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、氯气与水反应:Cl2+H2O=H++Cl-+HClO |
| C、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、钠和水反应:2Na+H2O=2Na++2OH-+H2↑ |
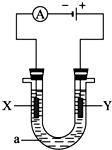 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题: