题目内容
11.下列说法正确的是( )| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | SiO2(s)+2C(s)=Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| C. | 常温下,NH4Cl溶液加水稀释,$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$增大 | |
| D. | C(s)+H2O(g)?CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 |
分析 A.电解法精炼铜时,以粗铜作阳极,失去电子;
B.SiO2(s)+2C(s)=Si(s)+2CO(g)中△S>0,常温下不能自发进行,则△H-T△S>0;
C.$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$=Kh,只与温度有关;
D.△H>0,为吸热反应,升高温度,正逆反应速率均增大,且平衡正向移动.
解答 解:A.电解法精炼铜时,以粗铜作阳极,失去电子,纯铜作阴极,阴极上铜离子得到电子,故A错误;
B.SiO2(s)+2C(s)=Si(s)+2CO(g)中△S>0,常温下不能自发进行,则△H-T△S>0,可知该反应的△H>0,故B正确;
C.$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$=Kh,只与温度有关,则常温下,NH4Cl溶液加水稀释,$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$不变,故C错误;
D.△H>0,为吸热反应,升高温度,正逆反应速率均增大,且平衡正向移动,逆反应速率不会减小,故D错误;
故选B.
点评 本题考查化学平衡移动、反应热与焓变,为高频考点,把握平衡移动的影响因素、反应进行方向的判断为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
2.某工业反应为:X2(g)+3Y2(g)?2XY3(g).图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响.

下列说法正确的是( )

下列说法正确的是( )
| A. | 由图Ⅰ可知,加入适当的催化剂,E和△H都减小 | |
| B. | 图Ⅱ中0~10 min内该反应的平均速率v(Y2)=0.045 mol•L-1•min-1,从11 min起其他条件不变,压缩容器的体积为1 L,则n(X2)的变化曲线为d | |
| C. | 图Ⅲ中a、b、c三点所处的平衡状态中,反应物X2的转化率最高的是b点 | |
| D. | 图Ⅲ中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则T1<T2,K1<K2 |
19.可逆反应X(g)+Y(g)?2N(g)(正反应为放热反应)从反应开始到t1 s达到平衡,在t2 s末由于条件改变,平衡被破坏,在t3 s末又建立新的平衡.图中表示上述变化过程中X和N的浓度(c)与反应时间的关系.在t2 s~t3 s之间的曲线变化是由下列哪种条件改变引起的( )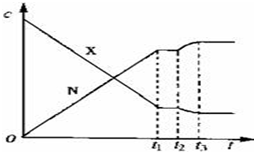

| A. | 降低温度 | B. | 增大N的浓度 | C. | 减小X的浓度 | D. | 增大压强 |
6.CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)?CH3OH中能说明上述反应在一定条件下一定达到最大限度的是( )
| A. | 反应物全部转化为甲醇 | |
| B. | 正反应和逆反应的化学反应速率均为零 | |
| C. | 反应体系中甲醇的百分含量不再变化 | |
| D. | CO和H2以1:1的物质的量之比反应生成甲醉 |
16.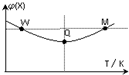 在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
 在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )| A. | 升高温度,平衡常数增大 | |
| B. | W点X的正反应速率小于M点X的正反应速率 | |
| C. | Q点时,Y的转化率最小 | |
| D. | 平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
1.一定温度下,可逆反应3X(g)+Y(g)?2Z(g)达到平衡的标志是( )
| A. | 单位时间内生成3n mol X,同时生成n mol Y | |
| B. | 2v逆(Y)=v正(Z) | |
| C. | X、Y、Z的浓度相等 | |
| D. | X、Y、Z的分子个数比为3:1:2 |