题目内容
某同学组装如图所示电化学装置,电极I为Zn,其它电极均为Cu。下列说法错误的是
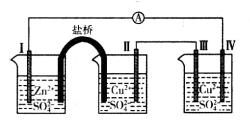
A.电极I发生氧化反应
B.相同的时间内,电极Ⅱ与Ⅳ质量变化相同
C.电极III的电极反应:4OH――4e-=2H2O+O2↑
D.电流方向:电极Ⅳ→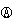 →电极I
→电极I
C
【解析】
试题分析:电极Ⅰ为Al,其它电极均为Cu,Al是活泼的金属易失电子作负极,及打击Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极。则 A、电极Ⅰ是负极,电极反应式为Al-3e-=Al3+,发生氧化反应,A正确;B、电极Ⅱ是正极,正极上发生反应为Cu 2++2e-=Cu,电极Ⅱ质量逐渐增大。电极Ⅳ是阴极,溶液中的铜离子放电,电极反应式为Cu 2++2e-=Cu,电极Ⅱ质量逐渐增大。根据电子转移守恒可知,电极Ⅱ与Ⅳ质量变化相同,B正确;C、电极Ⅲ为阳极,电极反应式为Cu-2e-=Cu 2+,C错误;D、原电池中电流从正极沿导线流向负极,即电极Ⅳ→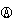 →电极Ⅰ,D正确,答案选C。
→电极Ⅰ,D正确,答案选C。
考点:考查电化学原理的应用

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案(14分)PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 | |
黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 |
PCl3 | —112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
(一)制备:下图是实验室制备PCl3的装置(部分仪器已省略)
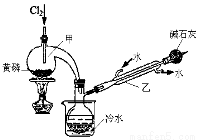
(1)仪器乙的名称 。
(2)实验室以制备Cl2的离子方程式: 。
(3)碱石灰的作用是 , 。
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间的CO2,其目的是 。
(二)提纯:
(5)粗产品品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到PCl3的纯品。
(三)分析:
测定产品中PCl3纯度的方法如下:迅速称取m g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1 mol/L V1 mL 碘溶液,充分反应后再用c2 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗V2 mL Na2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应。
(6)根据上述数据,该产品中PCl3的质量分数为 (用含字母的代数式表示、不必化简)。
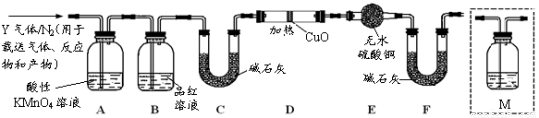


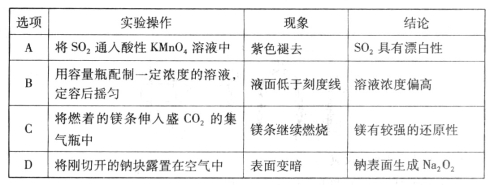
 2PCl3;2P+5Cl2(过量)
2PCl3;2P+5Cl2(过量)