题目内容
14.某有机物完全燃烧时只生成水和二氧化碳,且两者的物质的量之比为3:2,因而可以说( )| A. | 该有机物含碳、氢、氧三种元素 | |
| B. | 该化合物是乙烷 | |
| C. | 该化合物分子中碳、氢原子个数之比是1:3 | |
| D. | 该化合物分子中含2个碳原子,6个氢原子,但不能确定是否含氧分子 |
分析 某有机物完全燃烧时只生成水和二氧化碳,且两者的物质的量之比为3:2,则有机物一定含C、H元素,且H、C原子个数比为3×2:2=3:1,可能为乙烷或乙醇等,乙醇来解答.
解答 解:A.一定含C、H元素,可能含O元素,故A错误;
B.有机物中H、C原子个数比为3×2:2=3:1,可能为乙烷或乙醇,故B错误;
C.由水和二氧化碳的物质的量之比为3:2可知,该化合物分子中碳、氢原子个数之比是1:3,故C正确;
D.该有机物分子中一定不含氧分子,故D错误;
故选C.
点评 本题考查有机物分子式计算的确定,为高频考点,把握燃烧规律、原子守恒为解答的关键,侧重分析与计算能力的考查,注意有机物不一定为烃,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
2.1932年美国化学家鲍林首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,如表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是:自上而下电负性降低;
(2)预测周期表中电负性最大的元素应为F(写元素符号);估计钙元素的电负性的取值范围:0.8<X<1.2.
(3)简述元素电负性X的大小与元素金属性、非金属性之间的关系非金属性越强电负性越大,金属性越强电负性越小.
(4)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键.
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是:自上而下电负性降低;
(2)预测周期表中电负性最大的元素应为F(写元素符号);估计钙元素的电负性的取值范围:0.8<X<1.2.
(3)简述元素电负性X的大小与元素金属性、非金属性之间的关系非金属性越强电负性越大,金属性越强电负性越小.
(4)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键.
2.某有机物结构简式为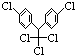 ,有关它的说法正确的是( )
,有关它的说法正确的是( )
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子中最多有23个原子共面 | ||
| C. | 分子式为C14H8Cl5 | D. | 1 mol该物质能与6 molH2加成 |
9.合成氨时能使合成氨反应进行程度增大的方法是( )
| A. | 升高温度 | B. | 降低压强 | C. | 使用催化剂 | D. | 及时分离出NH3 |
19.下列叙述正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| B. | 用相同的盐酸中和体积,物质的量浓度均相同的氢氧化钠和氨水溶液,所需盐酸的量相等 | |
| C. | 将氢氧化钠和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的50% | |
| D. | 氢氧化钠溶液的物质的量浓度是氨水的两倍,则氢氧化钠的OH-浓度也是氨水溶液的两倍 |
6.某无色透明溶液能与铝作用放出氢气,此溶液中一定能大量共存的离子组是( )
| A. | Cl-、SO42-、Na+、K+ | B. | K+、Fe2+、Na+、NO3- | ||
| C. | HCO3-、Na+、NO3-、K+ | D. | NO3-、Ba2+、Cl-、NH4+ |
3.下列各组数据中,前者刚好是后者两倍的是( )
| A. | 2 mol水的摩尔质量和1 mol水的摩尔质量 | |
| B. | 1 mol/L氯化钙溶液中n(Cl-)和2 mol/L氯化钾溶液中n(Cl-) | |
| C. | 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数 | |
| D. | 20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度 |