题目内容
某兴趣小组设计研究铜和稀硝酸反应速率V(NO)的实验。试回答下列问题:
(1)写出铜和稀硝酸反应的离子方程式___________________。
(2)为测定铜和稀硝酸反应速率v(NO),本实验需要记录的实验数据为:______________、___________。
(3)该兴趣小组间学对实验数据进行处理后得到用NO表示铜和稀硝酸的反应速率和时间的关系图如图所示.則:
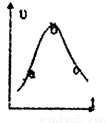
a—b,v(NO)变化的主要原因是___________________。
b→c,v(NO)变化的主要原因是___________________。
练习册系列答案
相关题目


 CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1.某科学实验将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图1所示(实线).图中数据a(1,6)代表的意思是:在1min时H2的物质的量是6mol。
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1.某科学实验将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图1所示(实线).图中数据a(1,6)代表的意思是:在1min时H2的物质的量是6mol。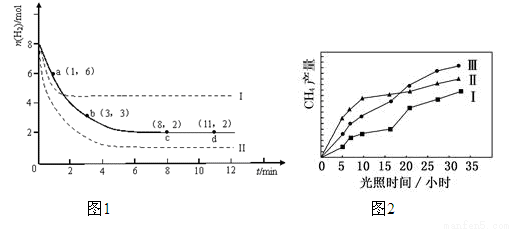
 CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增加的措施是
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增加的措施是