题目内容
1.25℃时,用浓度为0.1000mol/L的氢氧化钠溶液分别滴定20.00mL浓度均为0.l000mol/L的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断不正确的是( )| 数据编号 | 滴入NaOH(aq)的体积/mL | 溶液的pH | |
| HX | HY | ||
| ① | 0 | 3 | 1 |
| ② | a | 7 | x |
| ③ | 20.00 | >7 | y |
| A. | 在相同温度下,同浓度的两种酸溶液的导电能力:HX<HY | |
| B. | 由表中数据可估算出Ka(HX)≈10-5 | |
| C. | HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-) | |
| D. | 上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) |
分析 A.0.1000mol•L-1的酸HX、HY的pH分别为3、1,可知HX为弱酸、HY为强酸,溶液中离子浓度越大,导电能力越强;
B.0.100mol/L的HX溶液的pH=3,则c(H+)≈c(X-)=10-3mol/L,c(HX)=0.1mol/L-c(X-)≈0.1mol/L,再根据Ka(HX)=$\frac{c({H}^{+})×c({X}^{-})}{c(HX)}$计算;
C.溶液呈电中性,阳离子所带总电量等于阴离子所带总电量;
D.上述②反应后的HX溶液显中性,因为HX为弱酸,则a<20.00 mL,HY为强酸,与氢氧化钠反应时HY酸过量,溶液显酸性,c(H+)>c(OH-).
解答 解:A.0.1000mol•L-1的酸HX、HY的pH分别为3、1,可知HX为弱酸、HY为强酸,HY溶液中离子浓度更大,同浓度的两种酸溶液的导电能力顺序HX<HY,故A正确;
B.0.100mol/L的HX溶液的pH=3,则c(H+)≈c(X-)=10-3mol/L,c(HX)=0.1mol/L-c(X-)≈0.1mol/L,则Ka(HX)=$\frac{c({H}^{+})×c({X}^{-})}{c(HX)}$=$\frac{1{0}^{-3}×1{0}^{-3}}{0.1}$=10-5,故B正确;
C.HY和HX混合,根据电荷守恒:c(H+)=c(X-)+c(Y-)+c(OH-),故C正确;
D.上述②反应后的HX溶液显中性,因为HX为弱酸,则a<20.00 mL,由于HY为强酸,故HY酸过量,c(H+)>c(OH-),结合电荷守恒可知:c(Y-)>c(Na+),溶液中正确的离子浓度大小为:c(Y-)>c(Na+)>c(H+)>c(OH-),故D错误.
故选D.
点评 本题考查了酸碱混合的定性判断及离子浓度大小比较,题目难度中等,根据表中数据判断HX、HY的酸性强弱为解答关键,注意掌握电荷守恒、物料守恒的含义及在判断离子浓度大小中的应用,明确酸碱混合的定性判断方法及溶液pH的计算方法.

 优学名师名题系列答案
优学名师名题系列答案| A. | 250mL | B. | 375mL | C. | 475mL | D. | 500mL |
| A. | 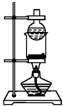 分离NaCl、I2混合物 | B. | 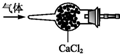 干燥CO2气体 | ||
| C. | 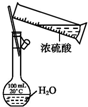 稀释浓硫酸 | D. | 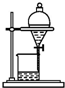 分离溴、CCl4混合物 |
| A. | c[NH3•H2O] | B. | c[H+] | C. | c[OH-] | D. | c[NH4+] |
| A. | 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将金属Li放于石蜡中密封保存 | |
| C. | 将NaOH溶液存放于磨口玻璃塞的试剂瓶 | |
| D. | 硝酸应装在棕色瓶中密封避光保存 |
| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 | |
| B. | 第二周期元素从Li到F,金属性逐渐减弱,非金属性逐渐增强 | |
| C. | 因为Na比K容易失去电子,所以Na比K的还原性强 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
| A. | 乙醇 | B. | 乙酸钠 | C. | 苯酚钠 | D. | 碳酸钠 |
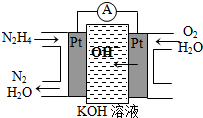 肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题 ;
;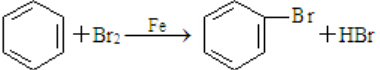 ;
;