题目内容
| |||||||||||||||||||

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案甲、乙两个研究性学习小组为测定氨分子张氮、氢原子个数比,设计了如下实验流程:

试验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。
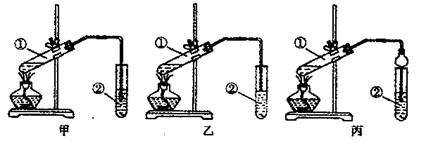
下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛,有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量为![]() 、氧化铜反应后剩余固体的质量为
、氧化铜反应后剩余固体的质量为![]()
![]() 生成氮气在标准状况下的体积
生成氮气在标准状况下的体积![]() 。
。
乙小组测得:洗气前装置D的质量![]() 、洗气后装置后D的质量
、洗气后装置后D的质量![]() 、生成氮气在标准状况下的体积
、生成氮气在标准状况下的体积![]() 。
。
请回答下列问题:
(1)写出仪器a的名称: 。
(2)检查A装置气密性的操作时 。
(3)甲、乙两小组选择了不同方法制取氨气,请将实验装置的字母编号和制备原理填写在下表空格中。
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③
|
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为 。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比名校小于理论值,其原因是 。 为此,乙小组在原有实验的基础上增加了一个装有药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出合理的实验结果。该药品的名称是 。
欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可采用以下四种方法。
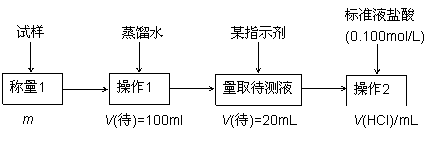
方法一:
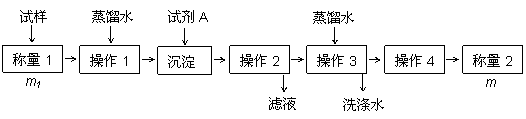
方法二:
 |
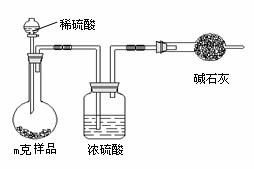
方法三:
 |
方法四:不使用化学试剂,使用实验室常用仪器。
按要求回答下列问题:
(1)方法一的操作1中要用到的玻璃仪器有烧杯、玻璃棒,还需要 ;操作2的名称是 ;该过程选择的指示剂是 ;该样品中NaHCO3的质量分数为 [用上图数据填写含m、V(HCl)的表达式]。
(2)方法二选择将HCO3- 离子转化为沉淀并称重,试剂A为 (填化学式)溶液;操作3的名称是 ;
如何判断这个目的已经达到: 。
(3)根据方法三中所用的实验装置,可判断需测定的实验数据是 ;仔细分析该实验装置,由此测得的数据计算出的实验结果有可能偏高也有可能偏低。
偏高的原因可能是 ;
偏低的原因可能是 。
(4)方法四的实验原理是 (用化学方程式表示)。