题目内容
14.选择恰当的试剂和采取的方法,除去下列物质中的少量杂质(括号内为杂质)(1)C2H6(C2H4)溴水、洗气
(2)溴苯(溴)氢氧化钠溶液、分液
(3)乙醇(水)氧化钙、蒸馏
(4)乙酸乙酯(乙酸)饱和碳酸钠溶液、分液.
分析 (1)乙烯与溴水反应,而乙烷不能;
(2)溴与NaOH溶液反应后,与溴苯分层;
(3)CaO与水反应后,增大与乙醇的沸点差异;
(4)乙酸与碳酸钠溶液反应后,与乙酸乙酯分层.
解答 解:(1)乙烯与溴水反应,而乙烷不能,则利用溴水、洗气分离,故答案为:溴水、洗气;
(2)溴与NaOH溶液反应后,与溴苯分层,则利用氢氧化钠溶液、分液分离,故答案为:氢氧化钠溶液、分液;
(3)CaO与水反应后,增大与乙醇的沸点差异,则利用氧化钙、蒸馏分离,故答案为:氧化钙、蒸馏;
(4)乙酸与碳酸钠溶液反应后,与乙酸乙酯分层,则选择饱和碳酸钠溶液、分液分离,故答案为:饱和碳酸钠溶液、分液.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应、混合物分离方法选择为解答的关键,侧重分析和应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
1.下列有关物质性质的应用正确的是( )
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 氯化钠是电解质,可电解其水溶液获得金属钠 | |
| C. | SO2有还原性,常用来漂白纸浆 | |
| D. | 四氯化碳密度比水大,可用于萃取溴水中的溴 |
5.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+NaHCO3═CaCO3↓+Na(NO3)2 | |
| D. | H++OH-═H2O 2KOH+H2SO4═K2SO4+2H2O |
9.下列化学用语正确的是( )
| A. | K+的结构示意图: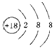 | B. | 四氯化碳的电子式: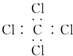 | ||
| C. | CH4分子的比例模型: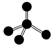 | D. | 过氧化氢结构式:H-O-O-H |
19.改变反应物用量,下列反应能用同一个反应方程式表示的是( )
①NaAlO2溶液与CO2反应; ②Si与烧碱溶液反应; ③H2S与NaOH溶液反应;
④Fe与稀硝酸反应; ⑤S在O2中燃烧; ⑥NH3与O2的反应.
①NaAlO2溶液与CO2反应; ②Si与烧碱溶液反应; ③H2S与NaOH溶液反应;
④Fe与稀硝酸反应; ⑤S在O2中燃烧; ⑥NH3与O2的反应.
| A. | ②⑤⑥ | B. | ①②③⑤ | C. | ①③④⑥ | D. | ①③④⑤⑥ |
6.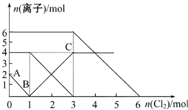 向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中正确的是( )| A. | 离子的还原性顺序为:Fe2+>Br->I- | |
| B. | 原混合溶液中FeBr2的物质的量为4mol | |
| C. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 | |
| D. | 当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
3.一定温度下,在恒容的密闭容器中,能表示反应:N2(g)+3H2(g)?2NH3(g)达到平衡状态的标志有( )
①容器中的压强不再发生变化
②H2的生成速率与NH3的消耗速率之比为3:2
③混合气的平均相对分子质量不变
④容器内混合气的密度不变
⑤NH3的物质的量浓度不再变化
⑥密闭容器中n(N2):n(H2):n(NH3)=1:3:2.
①容器中的压强不再发生变化
②H2的生成速率与NH3的消耗速率之比为3:2
③混合气的平均相对分子质量不变
④容器内混合气的密度不变
⑤NH3的物质的量浓度不再变化
⑥密闭容器中n(N2):n(H2):n(NH3)=1:3:2.
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③⑤ | D. | ②④⑥ |
4.下列描叙中,正确的是( )
| A. | Cl2以液态形式存在时可称作氯水或液氯 | |
| B. | 玛瑙的主要成分是二氧化硅 | |
| C. | 加碘食盐中所加的“碘”是KIO3 | |
| D. | 漂白粉的主要成分是次氯酸钙 |