题目内容
16.几种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性.下列说法不正确的是( )| M | N | ||
| X | Y |
| A. | 元素的第一电离能X<Y | |
| B. | X位于第三周期 IIA,其单质可采用电解熔融其氯代物制备 | |
| C. | 元素最高价氧化物的水化物中,酸性最强的是HNO3 | |
| D. | 气体分子(MN)2的电子式为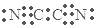 |
分析 Y的氧化物具有两性,Y为Al元素,结合位置可知,X为Mg,元素X的原子核外电子数是M的2倍,M为C,N为N,
A.Mg的3s电子全满为稳定结构;
B.Mg为活泼金属,电解法冶炼;
C.上述元素中N元素的非金属性最强;
D.(MN)2的结构式为N≡C-C≡N,均满足8电子稳定结构.
解答 解:Y的氧化物具有两性,Y为Al元素,结合位置可知,X为Mg,元素X的原子核外电子数是M的2倍,M为C,N为N,
A.Mg的3s电子全满为稳定结构,则元素的第一电离能X>Y,故A错误;
B.Mg为活泼金属,位于第三周期 IIA,其单质可采用电解熔融氯化镁制备,故B正确;
C.上述元素中N元素的非金属性最强,则元素最高价氧化物的水化物中,酸性最强的是HNO3,故C正确;
D.(MN)2的结构式为N≡C-C≡N,均满足8电子稳定结构,则电子式为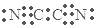 ,故D正确;
,故D正确;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
6.以下说法中正确的是( )
| A. | 测定溶液的酸碱度时,先将pH试纸用水润湿,后沾上被测溶液 | |
| B. | 点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃 | |
| C. | 实验室稀释浓硫酸时,可以在量筒中进行 | |
| D. | 试管和烧杯都可以直接用火焰加热 |
7.儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用.下列说法正确的是( )
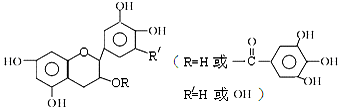

| A. | 儿茶素能与FeCl3溶液发生显色反应 | |
| B. | 1mol儿茶素最多可与10mol NaOH反应 | |
| C. | 常温下,儿茶素不溶于水,也不溶于有机溶剂 | |
| D. | 儿茶素一定不能发生水解反应 |
4.化学与生活、社会发展息息相关,下列有关说法不正确的是( )
| A. | 食盐可作调味剂,也可作食品防腐剂 | |
| B. | Na2O2和Na2O均可常用作呼吸面具中的供氧剂 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,是因为熬制过程发生了置换反应 | |
| D. | 古剑“沈卢”“以剂钢为刃”柔铁为蒸干,不尔则多断折”,剂钢是指铁合金 |
5.要防止水体污染,改善水质,最根本的措施是( )
| A. | 控制工业废水的排放 | B. | 对河水进行消毒处理 | ||
| C. | 控制农田排水 | D. | 减少用水量 |