题目内容
用如图装置测定工业碳酸钙的质量分数
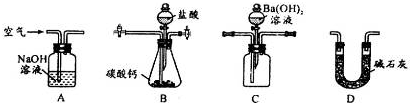
①按A-B-C-D顺序连接,然后从A装置通入空气,目的是 .
②装置D的作用为 .
③实验时,准确称取10.00g工业碳酸钙3份,进行3次测定,测得BaCO3沉淀的平均质量为17.73g,则样品中CaCO3的质量分数为 .若无D装置,测量结果则 .(填“偏大”、“偏小”、“无影响”)
④上述实验装置中,是否存在不合理之处? (填“是”或“否”);若有不合理之处,需改进的是 .

①按A-B-C-D顺序连接,然后从A装置通入空气,目的是
②装置D的作用为
③实验时,准确称取10.00g工业碳酸钙3份,进行3次测定,测得BaCO3沉淀的平均质量为17.73g,则样品中CaCO3的质量分数为
④上述实验装置中,是否存在不合理之处?
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:根据实验原理在B处利用盐酸与碳酸钙充分反应生成二氧化碳,到达C用氢氧化钡吸收,通过测得BaCO3沉淀的质量,结合碳守恒从而计算出碳酸钙的质量分数;为了保证实验的结果的准确性,增加了A装置,是通除了二氧化碳等酸性气体的空气让生成的二氧化碳全部放出,进入C装置被完全吸收,最后加D为了防止空气中的CO2与Ba(OH)2溶液反应,影响实验正确性,以此分析解答;
①根据实验原理,保证碳酸钙和盐酸反应产生的二氧化碳的放出是关键;
②碳酸钙和盐酸反应产生的二氧化碳的量不能受外界空气中二氧化碳和水的干扰;
③根据实验的原理结合化学反应进行计算即可;
④从能使分液漏斗的液体顺利流出,则必须搭建一个恒压漏斗,据此分析.
①根据实验原理,保证碳酸钙和盐酸反应产生的二氧化碳的放出是关键;
②碳酸钙和盐酸反应产生的二氧化碳的量不能受外界空气中二氧化碳和水的干扰;
③根据实验的原理结合化学反应进行计算即可;
④从能使分液漏斗的液体顺利流出,则必须搭建一个恒压漏斗,据此分析.
解答:
解:根据实验原理在B处利用盐酸与碳酸钙充分反应生成二氧化碳,到达C用氢氧化钡吸收,通过测得BaCO3沉淀的质量,结合碳守恒从而计算出碳酸钙的质量分数;为了保证实验的结果的准确性,增加了A装置,是通除了二氧化碳等酸性气体的空气让生成的二氧化碳全部放出,进入C装置被完全吸收,最后加D为了防止空气中的CO2与Ba(OH)2溶液反应,影响实验正确性;
①根据实验原理,保证碳酸钙和盐酸反应产生的二氧化碳的放出是关键,所以从A装置通入空气,目的是保证碳酸钙和盐酸反应产生的二氧化碳全部进入下一个装置,故答案为:让生成的二氧化碳全部放出,进入C装置,确保实验结果的准确性;
②碳酸钙和盐酸反应产生的二氧化碳的量不能受外界空气中二氧化碳和水的干扰,装置D的作用为防止空气中的CO2与Ba(OH)2溶液反应,故答案为:防止空气中的CO2与Ba(OH)2溶液反应;
③根据碳酸钙中碳元素守恒,碳酸钙中的碳元素先成为二氧化碳,然后是二氧化碳在和氢氧化钡反应得到碳酸钡沉淀,碳酸钡中的碳元素全部来自碳酸钙中,所以17.73gBaCO3沉淀的物质的量为
=0.09mol,所以碳酸钙的物质的量是0.09mol,质量是9g,百分含量是
×100%=90.00%;
若无D装置,则空气中的二氧化碳进入C中导致碳酸钡的质量偏大,所以碳酸钙也偏大,故测量结果则偏大;
故答案为:90.00%;偏大;
④因为随着分液漏斗中的液体流下,下面容器中的压强会变大,将会导致分液漏斗的液体不能顺利流下,所从在B、C装置中,为使分液漏斗中的液体顺利流出,用橡皮管将分液漏斗与锥形瓶、分液漏斗与集气瓶连接成连通装置能使分液漏斗的液体顺利流出,
故答案为:是;B、C装置中,为使分液漏斗中的液体顺利流出,用橡皮管将分液漏斗与锥形瓶、分液漏斗与集气瓶连接成连通装置.
①根据实验原理,保证碳酸钙和盐酸反应产生的二氧化碳的放出是关键,所以从A装置通入空气,目的是保证碳酸钙和盐酸反应产生的二氧化碳全部进入下一个装置,故答案为:让生成的二氧化碳全部放出,进入C装置,确保实验结果的准确性;
②碳酸钙和盐酸反应产生的二氧化碳的量不能受外界空气中二氧化碳和水的干扰,装置D的作用为防止空气中的CO2与Ba(OH)2溶液反应,故答案为:防止空气中的CO2与Ba(OH)2溶液反应;
③根据碳酸钙中碳元素守恒,碳酸钙中的碳元素先成为二氧化碳,然后是二氧化碳在和氢氧化钡反应得到碳酸钡沉淀,碳酸钡中的碳元素全部来自碳酸钙中,所以17.73gBaCO3沉淀的物质的量为
| 17.73g |
| 197g/mol |
| 9g |
| 10.00g |
若无D装置,则空气中的二氧化碳进入C中导致碳酸钡的质量偏大,所以碳酸钙也偏大,故测量结果则偏大;
故答案为:90.00%;偏大;
④因为随着分液漏斗中的液体流下,下面容器中的压强会变大,将会导致分液漏斗的液体不能顺利流下,所从在B、C装置中,为使分液漏斗中的液体顺利流出,用橡皮管将分液漏斗与锥形瓶、分液漏斗与集气瓶连接成连通装置能使分液漏斗的液体顺利流出,
故答案为:是;B、C装置中,为使分液漏斗中的液体顺利流出,用橡皮管将分液漏斗与锥形瓶、分液漏斗与集气瓶连接成连通装置.
点评:本题目是一道探究物质的含量的综合考查题,要求学生具有分析和解决问题的能力,难度大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
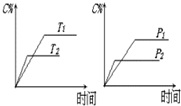 可逆反应a A(s)+b B(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图下列叙述正确的是( )
可逆反应a A(s)+b B(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图下列叙述正确的是( )| A、达平衡后,加入催化剂则C%增大 |
| B、达平衡后,若升温,平衡左移 |
| C、化学方程式中b<c+d |
| D、达平衡后,增加A的量有利于平衡向右移动 |
下列实验操作或数据合理的是( )
| A、用过滤的方法分离Fe(OH)3胶体和HCl溶液 |
| B、用托盘天平称取25.12gNaCl固体 |
| C、分别含有Mg2+、Cu2+和Na+的三种盐溶液,用NaOH溶液就能一次鉴别开 |
| D、从氯酸钾和二氧化锰制氧气后的混合物中分离出可溶物的操作步骤:溶解→过滤→蒸馏 |
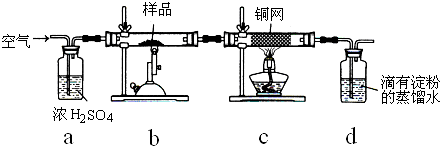
 (1)如图表示在密闭容器中反应:2SO2+O2?2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
(1)如图表示在密闭容器中反应:2SO2+O2?2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是