题目内容
设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,,则x + y =46
B.1 mol氯气参加氧化还原反应,一定得到NA 或2NA个电子
C.1升0.1 mol·L-1 NaBr溶液中,HBr和Br-总和为0.1NA个
D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
A
【解析】
试题分析:A、NO2和N2O4的最简式均是NO2,所以常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,则x + y =46,A正确;B、氯气在反应中也可能被氧化失去电子,B错误;C、溴化钠在溶液中不水解,不能存在溴化氢分子,C错误;D、浓硫酸与铜在反应过程中浓度逐渐降低,稀硫酸与铜不反应,所以12.5 mL 16 mol·L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA,D错误,答案选A。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
相关题目
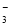 、NO
、NO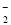 生成,则原溶液中一定含有_______,可能含有大量的________。
生成,则原溶液中一定含有_______,可能含有大量的________。

