题目内容
“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是( )
| A、活化分子之间的碰撞不一定都是有效碰撞 |
| B、升高温度,可使单位体积内活化分子数增多,反应速率加快 |
| C、催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
| D、对于有气体参加的反应增大压强,可使单位体积内活化分子百分数增加,反应速率加快 |
考点:活化能及其对化学反应速率的影响
专题:化学反应速率专题
分析:增大压强、浓度,单位体积活化分子的数目增多,升高温度、加入催化剂活化分子的百分数增大,分子间的有效碰撞几率增大,反应速率增大,据此分析.
解答:
解:A.能发生化学反应的碰撞叫做有效碰撞.只有具有一定能量的分子才有可能发生有效碰撞.因为分子发生碰撞时只有沿着一定的取向才能发生化学反应,所以,即便分子具有了发生有效碰撞的能量(即活化分子),发生的碰撞也不一定是有效碰撞,故A正确;
B.升高温度,使单位体积内活化分子数增多,活化分子的百分数增大,从而使有效碰撞次数增大,使化学反应速率增大,故B正确;
C.催化剂能降低反应的活化能,活化分子的百分数增大,从而使有效碰撞次数增大,故C正确;
D.对于有气体参加的反应,增大压强,活化分子的浓度增大,活化分子数目不变,反应速率加快,故D错误;
故选D.
B.升高温度,使单位体积内活化分子数增多,活化分子的百分数增大,从而使有效碰撞次数增大,使化学反应速率增大,故B正确;
C.催化剂能降低反应的活化能,活化分子的百分数增大,从而使有效碰撞次数增大,故C正确;
D.对于有气体参加的反应,增大压强,活化分子的浓度增大,活化分子数目不变,反应速率加快,故D错误;
故选D.
点评:本题考查有效碰撞与活化分子的关系,温度、压强、催化剂对活化分子和反应速率的影响,题目难度不大.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、化学变化中一定伴随着能量变化,伴随着能量变化的过程都是化学变化 |
| B、化石燃料和植物燃料燃烧时放出的能量均来自于太阳能 |
| C、光合作用中所发生的化学反应,反应物的总能量小于生成物的总能量 |
| D、放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定 |
下列说法正确的是( )
A、如图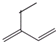 有机化合物主链5个C原子 有机化合物主链5个C原子 |
B、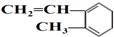 与Br2发生1:1加成反应的产物有6种 与Br2发生1:1加成反应的产物有6种 |
| C、苯的结构比较稳定,发生取代反应相对比较容易,发生苯环结构被破坏的加成反应困难得多,而氧化反应不能发生 |
D、丁苯橡胶结构如下,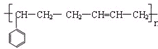 其单体均为烯烃 其单体均为烯烃 |
下列离子方程式正确的是( )
| A、溴化亚铁溶液与少量氯水混合:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
| B、向NaAlO2溶液中通入过量的CO2有白色沉淀:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32- |
| C、漂白液和强酸性洗涤剂混合使用:Cl-+ClO-+2H+=Cl2↑+H2O |
| D、少量碳酸氢镁与Ca(OH)2悬浊液混合:Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
根据热化学方程式(在25℃、101kPa时):S(s)+O2(g)=SO2(g)△H1=-297.23kJ/mol分析下列说法中一定正确的是( )
| A、S(s)的能量高于SO2(g)的能量 |
| B、S(s)和O2(g)的总能量大于SO2(g)的能量 |
| C、若有S(g)+O2(g)=SO2(g)△H2,则△H2>△H1 |
| D、形成1mol SO2(g)的化学键释放的总能量比断裂1mol S(s)和1mol O2(g)的化学键所吸收的总能量多297.23kJ |
检验溶液中是否含有某种离子,下列操作方法正确的是( )
| A、向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- |
| B、向某溶液中加稀 HCl,无明显现象,再加入BaCl2 溶液产生白色沉淀,证明有SO42- |
| C、向某溶液中加入稀 HCl,放出能使澄清的石灰水变浑浊的气体,证明有CO32 |
| D、把H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,证明H2O2有还原性 |
构成下列物质的原子不能共平面的是( )
| A、CH4 | B、乙烯 |
| C、乙炔 | D、苯 |