题目内容
11.称取45.8g某二价金属M的可溶性氢氧化物的水合晶体与Na2CO3•10H2O晶体的混合物,用蒸馏水全部溶解后过滤.得到的沉淀物经干燥后,称得质量为9.85g,高温灼烧此沉淀物,得到7.65g固体,在滤液中加入足量铵盐后加热,得到4.48dm3气体(标准状况).在此溶液中再加入盐酸,未见气体生成,求M的原子量及M的氢氧化物的水合晶体的化学式.分析 根据方程式MCO3$\frac{\underline{\;高温\;}}{\;}$MO+CO2↑来计算;根据所求结果结合题意:金属M的氢氧化物的水合晶体M(OH)2•xH2O与Na2CO3的混合物共45.8g来计算.
解答 解:设M的相对原子质量为m,则:MCO3$\frac{\underline{\;高温\;}}{\;}$MO+CO2↑
m+60 m+16
9.85 7.65
$\frac{m+60}{9.85}$=$\frac{m+16}{7.65}$,解得:m=137,
M是Ba,m(MCO3)=(137+60)×b=9.850,即b=0.05 mol,m(M(OH)2•xH2O)+m(Na2CO3)=45.8,
即(137+34+18x)×0.1+106×0.05=45.8,解得x=13,所以M氢氧化物的水合晶体的化学式为Ba(OH)2•13H2O,
答:M的原子量137,M的氢氧化物的水合晶体的化学式为Ba(OH)2•13H2O.
点评 本题考查学生根据化学方程式来确定物质以及量的多少的计算能力,注意平时知识的积累,难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
15.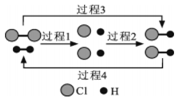 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )| A. | 过程 1 | B. | 过程 2 | C. | 过程 3 | D. | 过程 4 |
6.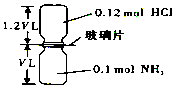 如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
 如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )| A. | 反应后瓶内压强是反应前的$\frac{1}{10}$ | |
| B. | 装置中氢元素的总质量为0.42g | |
| C. | 生成物的分子数目为0.1NA | |
| D. | 反应结束后,两个集气瓶很容易分开 |
3.关于下列各装置图的叙述不正确的是( )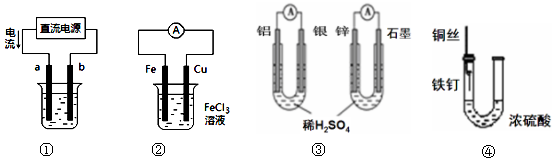

| A. | 用装置①精炼铜,则a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 图③两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 | |
| D. | 装置④中的铁钉几乎没被腐蚀 |
20.室温下,H2+Cl2$\stackrel{点燃}{→}$2HCl 生成 0.1mol HCl,下列说法正确的是( )
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
1.根据要求回答下列问题
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种
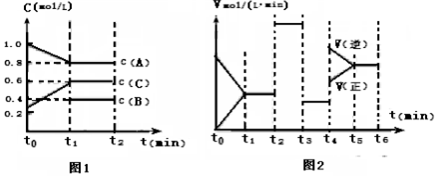
①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
K2> K4(填“>或<或.=”);其理由是t2-t4 平衡未移动,从图象知K4是温度升高平衡逆向移动后的常数,所以变小
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
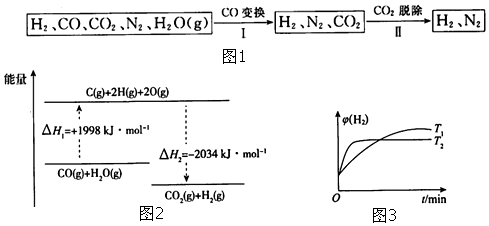
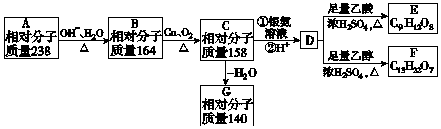
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种

①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
| 时间段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常数 | K1 | K2 | K3 | K4 |
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
 .
. .
. .
. 、
、 .
.