题目内容
某芳香族化合物A发生以下反应:(已知B的相对分子质量为108.有机玻璃的结构简式为 )
)

回答下列问题:
(1)A的分子式为 .
(2)G的结构简式 .
(3)B→D的反应类型 ,H→I的反应类型 .
(4)C→H的反应方程式 .D→E的反应方程式 .
(5)符合以下条件的M的同分异构体有 种(不包括M)
①含有苯环结构
②含有
写出其中一种的结构简式 .
 )
)
回答下列问题:
(1)A的分子式为
(2)G的结构简式
(3)B→D的反应类型
(4)C→H的反应方程式
(5)符合以下条件的M的同分异构体有
①含有苯环结构
②含有

写出其中一种的结构简式
考点:有机物的推断
专题:有机物的化学性质及推断
分析:根据机玻璃的结构简式,逆推可知,H为CH2=CHCOOCH3,C为CH2=CHCOOH,C与溴水发生加成反应得到G为BrCH2CH(Br)COOH,A在酸性条件下生成B与C,B氧化生成D,D能发生银镜反应,可推知,A应含有酯基,B中含有醇羟基、D含有-CHO,A为芳香族化合物,含有苯环,B的相对分子质量为108,去掉1个-OH、1个-C6H5剩余基团的式量=108-17-77=14,故剩余基团为CH2,可推知B为 ,故A为
,故A为 ,顺推可知,D为
,顺推可知,D为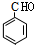 ,E为
,E为 、M为
、M为 、F为
、F为 ,据此解答.
,据此解答.
 ,故A为
,故A为 ,顺推可知,D为
,顺推可知,D为 ,E为
,E为 、M为
、M为 、F为
、F为 ,据此解答.
,据此解答.解答:
解:根据机玻璃的结构简式,逆推可知,H为CH2=CHCOOCH3,C为CH2=CHCOOH,C与溴水发生加成反应得到G为BrCH2CH(Br)COOH,A在酸性条件下生成B与C,B氧化生成D,D能发生银镜反应,可推知,A应含有酯基,B中含有醇羟基、D含有-CHO,A为芳香族化合物,含有苯环,B的相对分子质量为108,去掉1个-OH、1个-C6H5剩余基团的式量=108-17-77=14,故剩余基团为CH2,可推知B为 ,故A为
,故A为 ,顺推可知,D为
,顺推可知,D为 ,E为
,E为 、M为
、M为 、F为
、F为 ,
,
(1)由上述分析可知,A为 ,分子式为C10H10O2,
,分子式为C10H10O2,
故答案为:C10H10O2;
(2)G的结构简式为:BrCH2CH(Br)COOH,故答案为:BrCH2CH(Br)COOH;
(3)B→D是 发生催化氧化生成
发生催化氧化生成 ;
;
H→I是CH2=CHCOOCH3发生加聚反应生成 ,
,
故答案为:氧化反应;加聚反应;
(4)C→H的反应方程式为:CH2=CHCOOH+HOCH3
CH2=CHCOOCH3+H2O;
D→E的反应方程式为: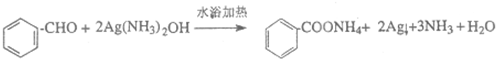 ,
,
故答案为:CH2=CHCOOH+HOCH3
CH2=CHCOOCH3+H2O; ;
;
(5)M为 的同分异构体,符合条件:①含有苯环结构,②含有
的同分异构体,符合条件:①含有苯环结构,②含有 ,只有1个侧链,可以为:-CH2COOH或-CH2OOCH,含有2个侧链,可以为:-CH3、-COOH或-CH3、-OOCH,各有邻、间、对三种位置关系,故符合条件的同分异构体有8种,其中一种的结构简式为:
,只有1个侧链,可以为:-CH2COOH或-CH2OOCH,含有2个侧链,可以为:-CH3、-COOH或-CH3、-OOCH,各有邻、间、对三种位置关系,故符合条件的同分异构体有8种,其中一种的结构简式为: 等,
等,
故答案为:8; 等.
等.
 ,故A为
,故A为 ,顺推可知,D为
,顺推可知,D为 ,E为
,E为 、M为
、M为 、F为
、F为 ,
,(1)由上述分析可知,A为
 ,分子式为C10H10O2,
,分子式为C10H10O2,故答案为:C10H10O2;
(2)G的结构简式为:BrCH2CH(Br)COOH,故答案为:BrCH2CH(Br)COOH;
(3)B→D是
 发生催化氧化生成
发生催化氧化生成 ;
;H→I是CH2=CHCOOCH3发生加聚反应生成
 ,
,故答案为:氧化反应;加聚反应;
(4)C→H的反应方程式为:CH2=CHCOOH+HOCH3
| 浓硫酸 |
| △ |
D→E的反应方程式为:
 ,
,故答案为:CH2=CHCOOH+HOCH3
| 浓硫酸 |
| △ |
 ;
;(5)M为
 的同分异构体,符合条件:①含有苯环结构,②含有
的同分异构体,符合条件:①含有苯环结构,②含有 ,只有1个侧链,可以为:-CH2COOH或-CH2OOCH,含有2个侧链,可以为:-CH3、-COOH或-CH3、-OOCH,各有邻、间、对三种位置关系,故符合条件的同分异构体有8种,其中一种的结构简式为:
,只有1个侧链,可以为:-CH2COOH或-CH2OOCH,含有2个侧链,可以为:-CH3、-COOH或-CH3、-OOCH,各有邻、间、对三种位置关系,故符合条件的同分异构体有8种,其中一种的结构简式为: 等,
等,故答案为:8;
 等.
等.
点评:本题考查有机物推断,注意根据有机玻璃的结构,采取正推法与逆推法相结合推断,能较好的考查学生的分析推理能力、有机化学基础,是常考题型,难度中等.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
分子式为C5H8O2,且既能与Na2CO3,溶液反应生成CO2,又能与溴的四氯化碳溶液反应的有机化合物有(不考虑立体异构)( )
| A、2种 | B、4种 | C、6种 | D、8种 |
在通常情况下,下列液体的pH大于7的是( )
| A、胃液 | B、食醋 |
| C、葡萄汁 | D、纯碱溶液 |
下列离子方程式书写正确的是( )
| A、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B、氢氧化钠溶液与硫酸铜溶液混合:Cu2++2OH-=Cu(OH)2↓ |
| C、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-=BaSO4↓ |
| D、金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ |