��Ŀ����
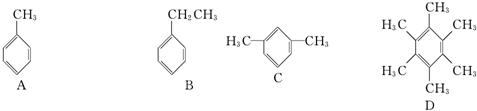
Mg���仯������Է�����ͼ1��ת�������ַ�Ӧ��������ˮ����ȥ������֪X��Y��ZΪ��̬���ʣ�B������ΪҺ̬��D����ɫΪ��ɫ��C��G���ð���̲�����A
��1��д���������ʵĻ�ѧʽ
A Y
��2�����õ���ʽ��ʾB���γɹ���
��3�����õ����ˮ��ƽ�����A+B+Mg��C+X+MgCl2��ԭ�� ��
��4����1molCO2ͨ��1L����ΪF����Һ�У���ַ�Ӧ��������Һ����εμ����ᣬ�����������������ɵ�����Ĺ�ϵ��ͼ2��ʾ����ԭF��Һ��Ũ��Ϊ mol/L��

��1��д���������ʵĻ�ѧʽ
A
��2�����õ���ʽ��ʾB���γɹ���
��3�����õ����ˮ��ƽ�����A+B+Mg��C+X+MgCl2��ԭ��
��4����1molCO2ͨ��1L����ΪF����Һ�У���ַ�Ӧ��������Һ����εμ����ᣬ�����������������ɵ�����Ĺ�ϵ��ͼ2��ʾ����ԭF��Һ��Ũ��Ϊ
���㣺������ƶ�
ר�⣺
������D����ɫ��ӦΪ��ɫ��˵������NaԪ�أ�D���Ȼ�þ��Ӧ�õ�������þ�����嵥��Y��E��E�к���NaԪ�أ����E�õ�F�����嵥��X��Z��X��Z��Ӧ�õ�G����G��������þ��Ӧ�õ��Ȼ�þ������֪GΪHCl��EΪNaCl��FΪNaOH����D��ˮ��Ӧ��������������Y���������������Ȼ�þ��Ӧ����������þ��E����DΪNa2O2��YΪO2��C��G���ð���̲�����A����CΪNH3��AΪNH4Cl��B������ΪҺ̬��A��B��Mg��ϵõ��������Ȼ�þ��X����BΪH2O��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬�����ݳ�NH3����XΪH2����ZΪCl2���ݴ˽��
���
�⣺D����ɫ��ӦΪ��ɫ��˵������NaԪ�أ�D���Ȼ�þ��Ӧ�õ�������þ�����嵥��Y��E��E�к���NaԪ�أ����E�õ�F�����嵥��X��Z��X��Z��Ӧ�õ�G����G��������þ��Ӧ�õ��Ȼ�þ������֪GΪHCl��EΪNaCl��FΪNaOH����D��ˮ��Ӧ��������������Y���������������Ȼ�þ��Ӧ����������þ��E����DΪNa2O2��YΪO2��C��G���ð���̲�����A����CΪNH3��AΪNH4Cl��B������ΪҺ̬��A��B��Mg��ϵõ��������Ȼ�þ��X����BΪH2O��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬�����ݳ�NH3����XΪH2����ZΪCl2��
��1��������������֪��AΪNH4Cl��YΪO2���ʴ�Ϊ��NH4Cl��O2��
��2��BΪH2O���õ���ʽ��ʾˮ���γɹ���Ϊ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��A+B+Mg��C+X+MgCl2�Ļ�ѧ����ʽΪ2NH4Cl+Mg=2NH3��+H2��+MgCl2��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬��Ӧ�ų����������ݳ�NH3��
�ʴ�Ϊ��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬�����ݳ�NH3��
��4����������̼���������Ʒ�Ӧֻ����̼���ƣ��ټ������ᣬ������Ӧ��Na2CO3+HCl=NaCl+NaHCO3��NaHCO3+HCl=NaCl+CO2��+H2O��ǰ�������������������֮��Ϊ1��1����ʵ��ǰ�������������������֮��Ϊ2��1���ʶ�����̼��NaOH��Ӧ��NaOH��ʣ�࣬�õ�NaOH��Na2CO3�����Һ������̼Ԫ���غ��֪��n��NaHCO3��=n��CO2��=1mol����NaHCO3+HCl=NaCl+CO2��+H2O����֪�ܽ�̼����������n��HCl��=n��NaHCO3��=1mol�������������Ϊ30mL-20mL=10mL������ΪNaCl��Һ�����������ܹ�����30mL���ᣬ�����������ܹ�����HClΪ1mol��
=3mol�������������غ㣬������NaClΪ3mol�����������غ��֪n��NaOH��=n��NaCl��=3mol����NaOH��ҺŨ��Ϊ
=3mol/L���ʴ�Ϊ��3��
��1��������������֪��AΪNH4Cl��YΪO2���ʴ�Ϊ��NH4Cl��O2��
��2��BΪH2O���õ���ʽ��ʾˮ���γɹ���Ϊ
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����3��A+B+Mg��C+X+MgCl2�Ļ�ѧ����ʽΪ2NH4Cl+Mg=2NH3��+H2��+MgCl2��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬��Ӧ�ų����������ݳ�NH3��
�ʴ�Ϊ��NH4Clˮ������NH3?H2O��HCl������þ����Ϊþ�dz����ã���ˮ���������ᷴӦ����H2��ʹ��Һ�������ӵ�Ũ�ȼ�С���Ӷ��ٽ���NH4Cl��ˮ�⣬�����ݳ�NH3��
��4����������̼���������Ʒ�Ӧֻ����̼���ƣ��ټ������ᣬ������Ӧ��Na2CO3+HCl=NaCl+NaHCO3��NaHCO3+HCl=NaCl+CO2��+H2O��ǰ�������������������֮��Ϊ1��1����ʵ��ǰ�������������������֮��Ϊ2��1���ʶ�����̼��NaOH��Ӧ��NaOH��ʣ�࣬�õ�NaOH��Na2CO3�����Һ������̼Ԫ���غ��֪��n��NaHCO3��=n��CO2��=1mol����NaHCO3+HCl=NaCl+CO2��+H2O����֪�ܽ�̼����������n��HCl��=n��NaHCO3��=1mol�������������Ϊ30mL-20mL=10mL������ΪNaCl��Һ�����������ܹ�����30mL���ᣬ�����������ܹ�����HClΪ1mol��
| 30mL |
| 10mL |
| 3mol |
| 1L |
���������⿼�������ƶϡ���ѧͼ���йؼ��㣬��Ŀ�ۺ��Խ�ǿ���ԡ�D����ɫ��Ӧ��G��������þ�ķ�Ӧ��Ϊͻ�ƿڽ����ƶϣ�ע����Ŀʡ�Բμӷ�Ӧ��ˮ����Ҫѧ����������Ԫ�ػ��������ʡ���ѧ��Ӧԭ���ȣ���Ŀ�ۺ���ǿ���Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
��ͼ����ȡ���ռ�ij�����ʵ��װ�ã������ڣ�������
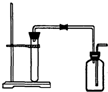

| A����Zn����ϡHCl��Ӧ��H2 |
| B����Na2O2��H2O��Ӧ��O2 |
| C����Cu��ϡHNO3��Ӧ��NO |
| D����MnO2��ŨHCl��Ӧ��Cl2 |
�����й����߷��Ӳ���Ӧ�õ�˵������ȷ���ǣ�������
| A���߷���Ĥ������ѡ�����������������ں�ˮ��������Ⱦ���ơ�������ȡ����յȷ��� |
| B����Ϊҽ�ø߷��Ӳ������������٣����뿼����������������Ժͻ�е���� |
| C�����͵ľ���ϩ������ˮ�Ը߷��ӣ�������ˮ�����ӷ�������ԣ����Գ�Ϊ����ʪ�� |
| D���²����о��������ܻ����߹��ܵķ���չ |
��Ȼά����P���ṹ��ͼ�������ڻ��������У�����һ��Ӫ��������������ά����P������������ǣ�������
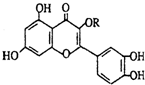

| A�����Ժ���ˮ��Ӧ |
| B���������л��ܼ� |
| C�����л���������Ա����� |
| D��1molά����P�����Ժ�4molNaOH��Ӧ |
��ѧ������������������أ������й�������ȷ���ǣ�������
| A��������ǡ���Ϣ��������֧�����ϣ����������ά |
| B�����������ֹ������ֱ����Դ�����������Ա��������ܸ�ʴ |
| C����ѧ��Ӧ�����������ı仯����Ӧ��������һ������������������ |
| D���ý��ݹ����������Һ�Ĺ���������ˮ���ͷŵ���ϩ���ɴﵽˮ�����ʵ�Ŀ�� |