题目内容
类似于水的离子积,难溶盐AmBn也有离子积Ksp,且Ksp=[c(An+)]m?[c(Bm-)]n,已知常温下BaSO4的溶解度为2.33×10-4g,则其Ksp为( )
| A、2.33×10-4 |
| B、1×10-5 |
| C、1×10-10 |
| D、1×10-12 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:依据溶解度计算出硫酸钡的物质的量,然后计算钡离子和硫酸根的浓度,然后依据公式计算即可.
解答:
解:硫酸钡的相对分子质量为:233,故硫酸钡的物质的量为:
=1.0×10-6mol,100g水中溶解2.33g溶剂,故溶液的体积约为100mL,即0.1L,故c(SO42-)=c(Ba2+)=c(BaSO4)=
1.0×10-5mol/L,故BaSO4的Ksp=1.0×10-5mol/L×1.0×10-5mol/L=1.0×10-10mol2/L2,
故选C.
| 2.33×10-4g |
| 233g/mol |
| 1.0×10-6mol |
| 0.1L |
故选C.
点评:本题主要考查的是难溶电解质的溶度积的计算,正确掌握公式是解决本题的关键,属于常考题.

练习册系列答案
 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
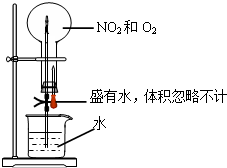 用如图所示的装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑2NO2?N2O4.最终液体充满了烧瓶,则烧瓶内溶液的物质的量浓度约是( )
用如图所示的装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑2NO2?N2O4.最终液体充满了烧瓶,则烧瓶内溶液的物质的量浓度约是( )A、
| ||
B、
| ||
C、
| ||
| D、无法计算 |
下列说法正确的是( )
| A、难溶电解质的溶度积越小,溶解度越大 |
| B、可以通过沉淀反应使杂质离子完全沉淀 |
| C、难溶电解质的溶解达到平衡后就静止不动了 |
| D、一定浓度的NH4Cl溶液可以溶解Mg(OH)2 |
常温下,AgI的溶度积是8.3×10-17,在该温度下把0.01L浓度为8.0×10-6mol/L的AgNO3溶液和0.01L浓度为4.0×10-7 mol/L的KI溶液混合,下列说法正确的是(溶液体积变化忽略不计)( )
| A、不能确定有无AgI沉淀生成 |
| B、没有AgI沉淀生成 |
| C、有KNO3晶体析出 |
| D、有AgI沉淀生成 |
若溶液中由水电离产生的c(OH-)=1×10-12 mol?L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A、Al3+ Na+ NO3- Cl- |
| B、K+ Na+ Cl- NO3- |
| C、K+ Na+ Cl- CO32- |
| D、K+ NH4+ SO42- NO3- |
电解CuSO4溶液时,要求达到三点(1)阳极质量减少;(2)阴极质量增加;(3)电解质溶液中c(Cu2+)不变,则可选用的电极是( )
| A、纯铜作阳极,含Zn和Ag的铜合金作阴极 |
| B、含Zn和Ag的铜合金作阳极,纯铜作阴极 |
| C、用纯铁作阳极,纯铜作阴极 |
| D、用石墨作阳极,纯铜作阴极 |
可逆反应 mA(气)+nB(气)?pC(气)+qD(气),在密闭容器中反应达到平衡,改变某一条件后,正反应速率增大,则下列说法正确的是( )
| A、A的转化率增大 |
| B、平衡向逆反应方向移动 |
| C、平衡没有移动 |
| D、上述三种情况都有可能 |
