题目内容
5.能正确表示下列反应的离子方程式是( )| A. | 金属铝溶于稀硫酸中:Al+2H+═Al3++H2↑ | |
| B. | 碳酸锌溶于稀硝酸中:CO32-+2H+═H2O+CO2↑ | |
| C. | 氢氧化铝中和胃酸:OH-+H+═H2O | |
| D. | 少量Cl2通入KI溶液中:Cl2+2I-═2Cl-+I2 |
分析 A.电荷不守恒;
B.碳酸锌为沉淀,应保留化学式;
C.氢氧化铝为沉淀,应保留化学式;
D.氯气与碘化钾反应生成氯化钾和碘;
解答 解:A.金属铝溶于稀硫酸中,离子方程式:2Al+6H+═2Al3++3H2↑,故A错误;
B.碳酸锌溶于稀硝酸中,离子方程式:ZnCO3+2H+═H2O+CO2↑+Zn2+,故B错误;
C.氢氧化铝中和胃酸,离子方程式:Al(OH)3+3H+═3H2O+Al3+,故C错误;
D.少量Cl2通入KI溶液中,离子方程式:Cl2+2I-═2Cl-+I2,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循原子个数守恒、遵循电荷守恒,注意化学式的拆分,题目难度不大.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
15.下列各组中两个化学反应,属于同一反应类型的一组是( )
| A. | 由苯制硝基苯;由苯制环己烷 | |
| B. | 由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷 | |
| C. | 乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 由苯制溴苯;CH4制CH2Cl2 |
16.下列物质属于烷烃的是( )
| A. | CH3CH2OH | B. | CO | C. | 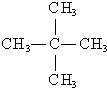 | D. | CH2═CH-CH3 |
13.在溶液中能大量共存的一组离子或分子是( )
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、AlO2-、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、ClO- | D. | Al3+、CH3COO-、SO42-、H+ |
20.下列关于电解质溶液的叙述正确的是( )
| A. | 在pH=3的溶液中,Na+、Cl-、Fe2+、ClO-可以大量共存 | |
| B. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| C. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)增大 |
10.将7.4gNa2CO3•10H2O和NaHCO3组成的混合物完全溶解于水配成100mL溶液,测得溶液中c(Na+)=0.6mol/L.若将等质量的混合物与过量盐酸反应后加热蒸干,可以得到固体的质量是( )
| A. | 3.12g | B. | 3.51g | C. | 5.02g | D. | 无法计算 |
17.下列气体,能使紫色石蕊试剂先变红后褪色的是( )
| A. | CO2 | B. | 氯气 | C. | O3 | D. | SO2 |
15.下列有关晶体的说法中,不正确的是( )
| A. | 晶体中一定存在化学键 | |
| B. | 已知晶胞的组成就可推知晶体的组成 | |
| C. | 分子晶体在晶体态或熔融态下均不导电 | |
| D. | 原子晶体中只存在共价键,不可能存在其他类型的化学键 |
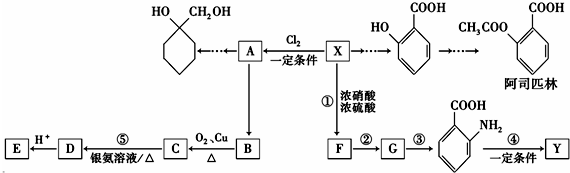

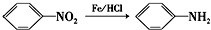 (苯胺,易被氧化)
(苯胺,易被氧化)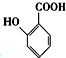 中官能团名称为酚羟基、羧基;
中官能团名称为酚羟基、羧基; ;
; $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$  +(n-1)H2O;
+(n-1)H2O; 的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2
的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2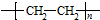
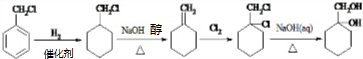 .
.