题目内容
关于电子云的下列说法不正确的是( )
| A、s电子绕核旋转,其轨道为一圆圈,而p电子是走∞字形 |
| B、s轨道都是球形轨道 |
| C、轨道不同,电子云的取向不一样 |
| D、电子云图是形象地描述电子在空间单位体积内出现概率大小的图形 |
考点:原子核外电子的运动状态
专题:原子组成与结构专题
分析:电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形,其运动规律跟一般物体不同,它没有明确的轨道.s电子云,是球形对称的,在核外半径相同处任一方向上电子出现的几率相同,轨道不同的,电子与的取向不同,据此解答.
解答:
解:A.电子没有固定的轨道,故A错误;
B.s电子云,是球形对称的,s轨道都是球形轨道,故B正确;
C.轨道不同,电子云的取向不一样,故C正确;
D.电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形,故D正确;
故选:A.
B.s电子云,是球形对称的,s轨道都是球形轨道,故B正确;
C.轨道不同,电子云的取向不一样,故C正确;
D.电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形,故D正确;
故选:A.
点评:本题考查了电子云,明确电子云的定义是解题的关键,注意不同轨道的电子,电子云的取向不同.

练习册系列答案
相关题目
下列可逆反应一定处于平衡状态的是( )
| A、2HBr(g)?Br2 (g)+H2 (g),固定反应容器中压强不再改变. |
| B、N2(g)+3H2 (g)?2 NH3 (g) 测得正反应速率υ(N2)=0.01 mol?L-1?min-1,逆反应速率υ,(NH3 )=0.01 mol?L-1?mⅠn-1 |
| C、2SO2 (g)+O2 (g)?2SO3(g),在 t1和t2 时刻SO2 的转化率为 40% |
| D、2CO(g)+O2(g)?2CO2(g),测得混合物中CO、O2和CO2的物质的量之比为 2:1:1 |
关于如图所示各装置的叙述中,正确的是( )
A、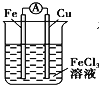 是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
B、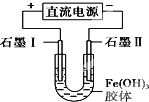 通电一段时间后石墨Ⅱ电极附近溶液红褐色加深 |
C、若用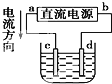 精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
D、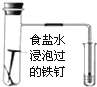 研究的是金属的析氢腐蚀,Fe上的反应为Fe-2e-=Fe2+ |
设NA代表阿伏加德罗常数的数值,下列说法不正确的是( )
| A、36g镁在足量的二氧化碳气体中完全燃烧共转移的电子数为3NA |
| B、1L 1mol?L-1的Na2CO3溶液中含有Na+的数目为NA |
| C、标准状况下,2.24L CO2和SO2混合气体中含有的氧原子数目为0.2NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质.下列各项的事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能使酸性高锰酸钾褪色 |
| B、乙烯能与溴水发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚与溴水可直接反应,而苯与液溴反应则需要铁作催化剂 |
| D、苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
下列化学用语书写正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、丙烯的键线式: |
C、CH4分子的比例模型: |
D、乙醇的结构式: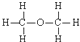 |
下列判断不合理的是( )
| A、能电离出H+的物质不一定是酸 |
| B、蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液 |
| D、焰色反应是化学变化 |